Tematiche - Corrosione
261.0.053 / V8
3 Tipi di corrosione
In tutti i processi di corrosione elettrolitica, il processo anodico è sempre una dissoluzione del metallo (ossidazione). Il processo catodico (riduzione) può invece essere causato da svariate reazioni. Il tipo di corrosione viene spesso denominato in funzione dell’agente riducente o dell’agente ossidante.
3.1 Corrosione ad alta temperatura
La corrosione ad alta temperatura dei metalli avviene in combinazione con gas secchi, senza il coinvolgimento di un elettrolita. Le corrispondenti reazioni di ossidazione e riduzione avvengono a temperature di ca. 400 °C e oltre.
Nell’ossidazione dei metalli con gas quali l’ossigeno, sulle superfici metalliche si formano strati di ossido metallico più o meno stabili. Un esempio di corrosione ad alta temperatura è l’incrostazione delle superfici metalliche durante la lavorazione dei metalli.
Poiché tutti i casi di corrosione sono dovuti a cause elettrochimiche, la corrosione ad alta temperatura non viene ulteriormente descritta nel presente documento.
3.2 Corrosione da ossigeno
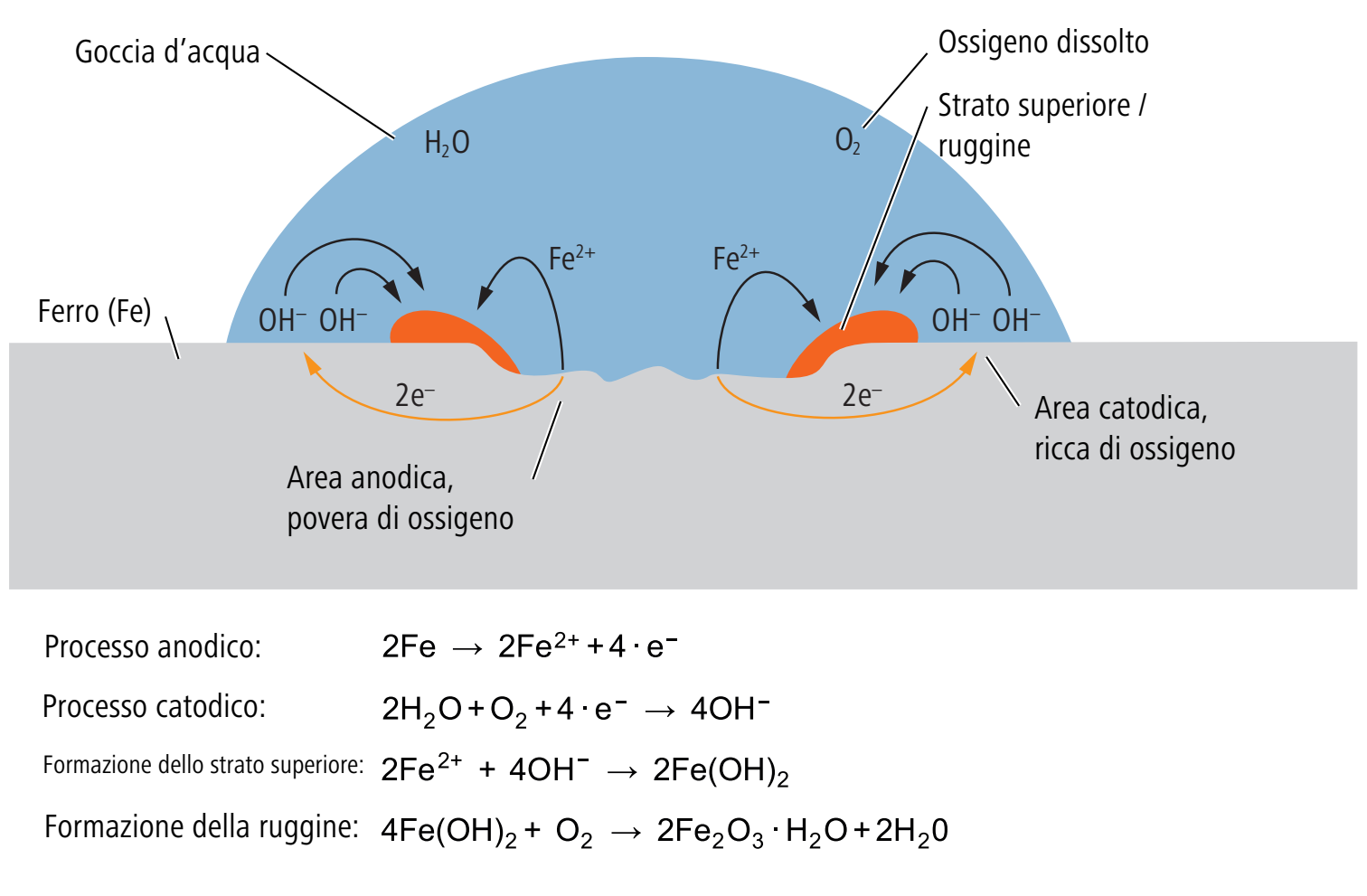
La corrosione da ossigeno è il tipo di corrosione più frequente a causa della presenza di ossigeno nell’aria e dei suoi valori di potenziale sempre fortemente positivi. Nella corrosione da ossigeno, il processo catodico consiste nella riduzione dell’ossigeno a ioni di ossigeno. La corrosione da ossigeno si verifica già a diverse concentrazioni di elettroliti che formano un elemento di concentrazione, ad esempio in una goccia d’acqua su una superficie di ferro.
Il processo catodico si svolge quindi nella zona periferica della goccia d’acqua dove la concentrazione di ossigeno è più elevata. Nella zona centrale avviene la dissoluzione del metallo (processo anodico) che innesca ulteriori reazioni e porta infine alla formazione della ruggine.
La corrosione da ossigeno si verifica soprattutto in elettroliti neutri o alcalini con valore di pH > 7. Negli elettroliti acidi (pH < 7), la corrosione da ossigeno è sostituita dalla corrosione da idrogeno a causa della predominanza di quest’ultimo nell’elettrolita. Tutti i metalli il cui potenziale è inferiore a quello dell’ossigeno possono essere attaccati dalla corrosione da ossigeno.
3.3 Corrosione da idrogeno
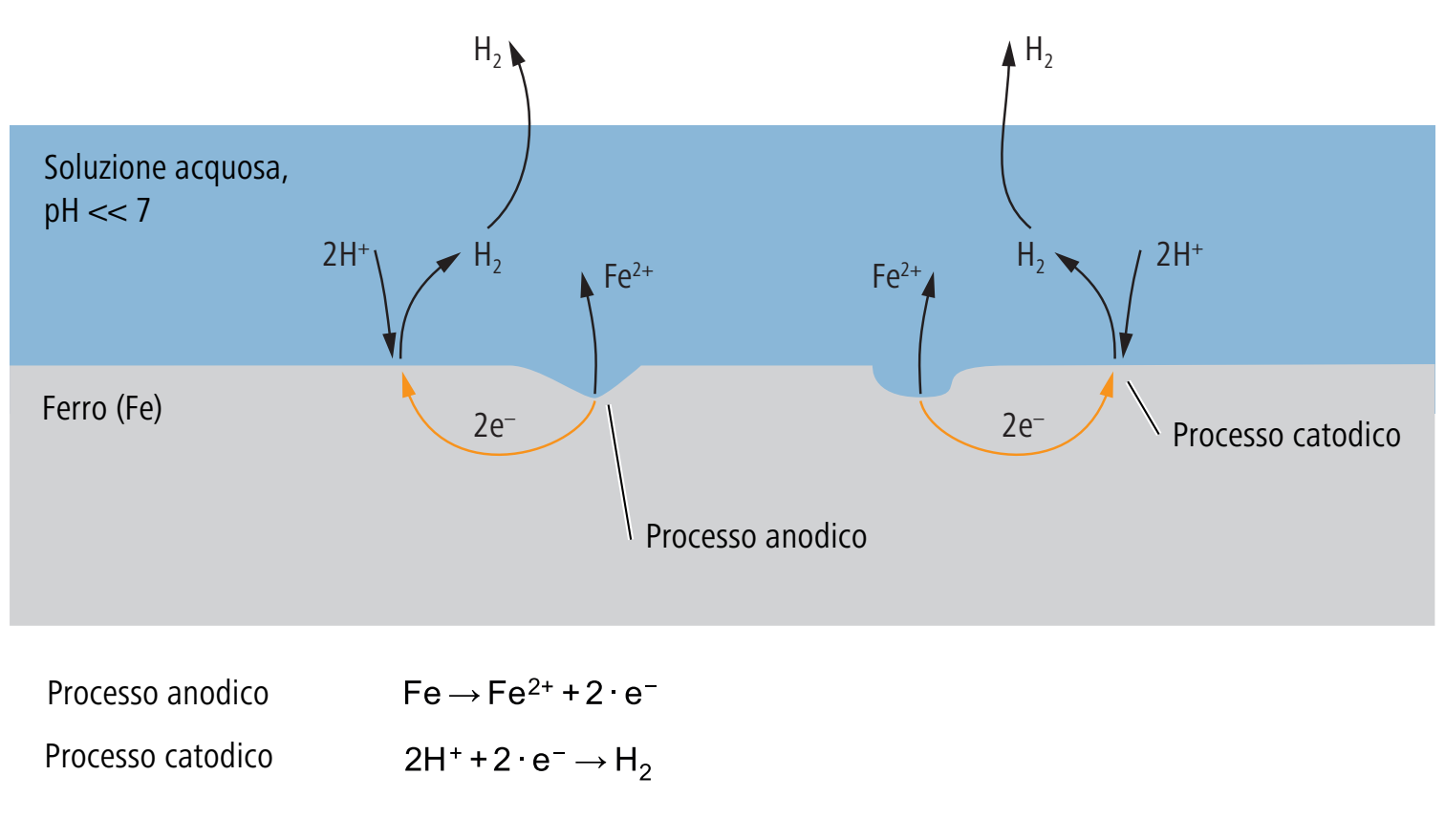
La corrosione da idrogeno avviene in soluzioni fortemente acide, anche in completa assenza di ossigeno. Tali soluzioni hanno bassi valori di pH e presentano elevate concentrazioni di idrogeno.
Nella corrosione da idrogeno, il processo catodico consiste nella riduzione degli ioni di idrogeno H+ in idrogeno gassoso H2. Il processo anodico consiste, come in tutti i tipi di corrosione, nella dissoluzione del metallo attraverso il rilascio di elettroni dal reticolo metallico e nella formazione di ioni metallici. I processi anodici e catodici avvengono sull’intera superficie metallica in punti e momenti diversi. Nella corrosione da idrogeno non è possibile individuare l’anodo e il catodo.
I metalli comuni immersi in soluzioni acquose fortemente acide sono esposti alla corrosione sia da idrogeno sia da ossigeno, mentre i metalli nobili subiscono la corrosione da idrogeno solo in soluzioni acquose con bassi valori di pH. Ciò conferma l’esperienza che gli acidi hanno un effetto più aggressivo rispetto a quello degli alcali.
3.4 Corrosione bimetallica
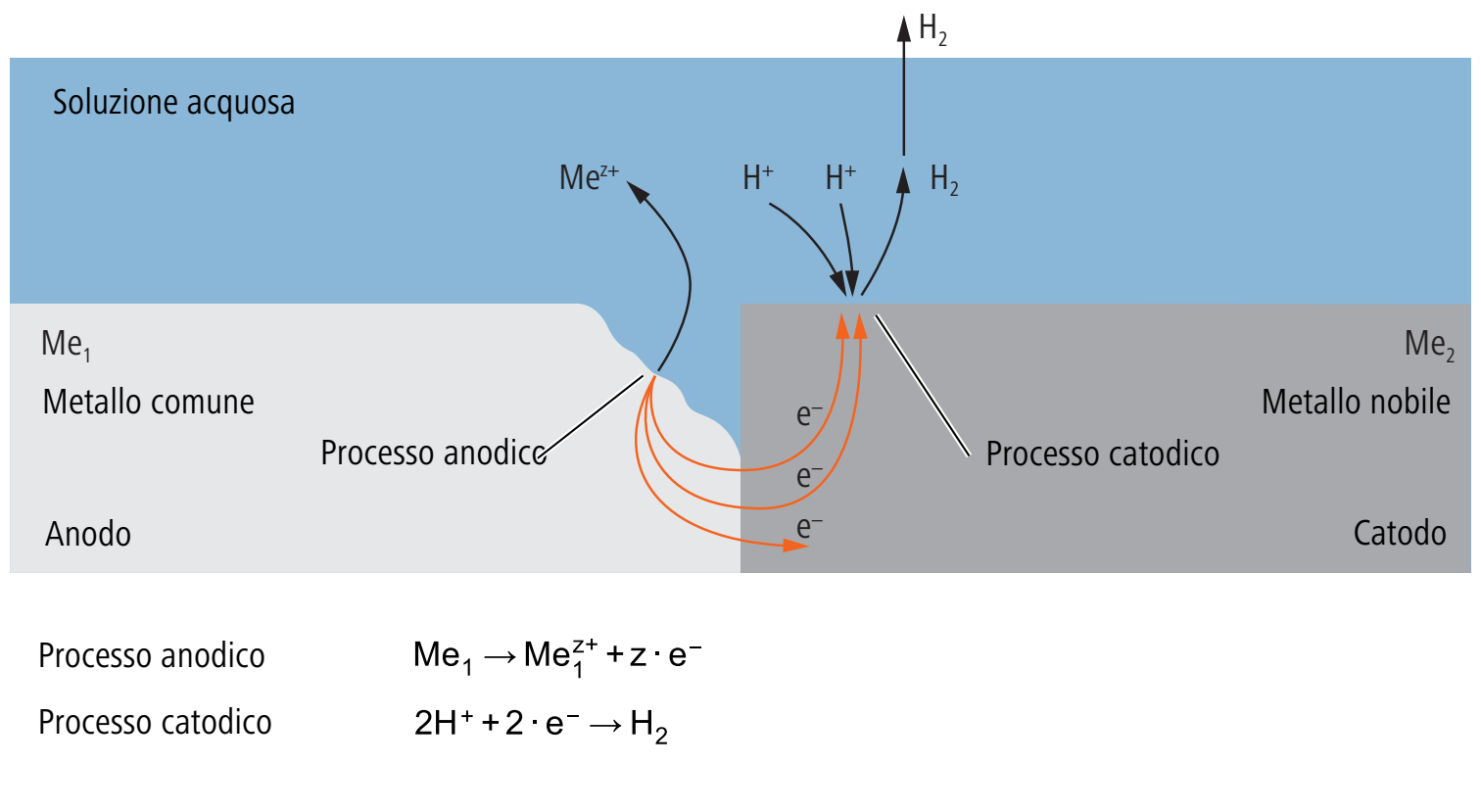
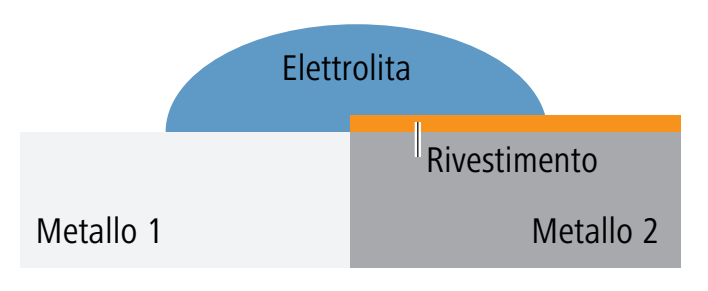
La corrosione bimetallica si verifica quando metalli con potenziali elettrochimici diversi formano un elemento galvanico cortocircuitato in presenza di una soluzione acquosa, per cui il metallo meno nobile viene attaccato in modo corrosivo.
L’immagine mostra la riduzione dell’idrogeno come processo catodico ma è possibile anche la riduzione dell’ossigeno.
I fattori d’influenza seguenti incrementano la corrosione bimetallica:
-
Marcata differenza di potenziale dei metalli
-
Elevata conducibilità dei metalli e dell’elettrolita
-
Elevata conducibilità della superficie di contatto tra i metalli
Da quanto sopra si possono derivare relative misure per ridurre la corrosione bimetallica, ad esempio evitare le installazioni miste o l’isolamento elettrico dei metalli.
Nell’impianto di acqua potabile, il contatto metallico tra i componenti delle condutture in materiali metallici diversi e l’acqua potabile e/o lʼacqua di condensa che funge da elettrolita crea un elemento di corrosione nei punti di contatto. Vi è un flusso di corrente di corrosione.
3.4.1 Immagini del danno
La seguente immagine del danno mostra la corrosione bimetallica su una tubazione. La corrosione bimetallica è stata causata da braccialetti inadeguati.
L’immagine seguente mostra la corrosione bimetallica su un fitting in condizioni di laboratorio. La corrosione bimetallica è stata causata da una combinazione di materiali: tubo in acciaio inossidabile e fitting in acciaio al carbonio. La corrosione bimetallica non è direttamente visibile nell’immagine ma solo i prodotti della corrosione sotto forma di depositi biancastri.
3.4.2 Evitare la corrosione bimetallica
La corrosione bimetallica può essere evitata in vari modi con accorgimenti strutturali, da un lato riducendo al minimo la differenza di potenziale elettrochimico dei materiali, dall’altro prevenendo le correnti di corrosione.
La tabella seguente mostra in modo schematico come evitare la corrosione bimetallica:
|
Immagine |
Descrizione |
|---|---|
|
|
La corrente di corrosione viene impedita da un elemento costruttivo a isolamento elettrico, ad esempio la bussola a colletto 90056 o il raccordo isolante Optipress-Aquaplus 81042. |
|
|
Un rivestimento o uno strato passivo su una superficie metallica impedisce la formazione di corrente di corrosione, ad esempio la fascia 83204 o l’acciaio inossidabile come materiale. |
|
|
La struttura è realizzata con metalli con potenziale elettrochimico approssimativamente uguale oppure si evitano le cosiddette installazioni miste. |
|
|
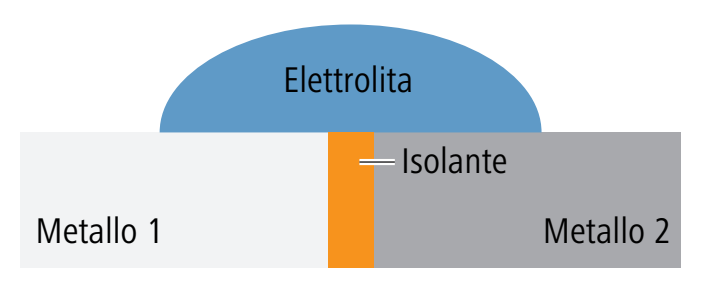
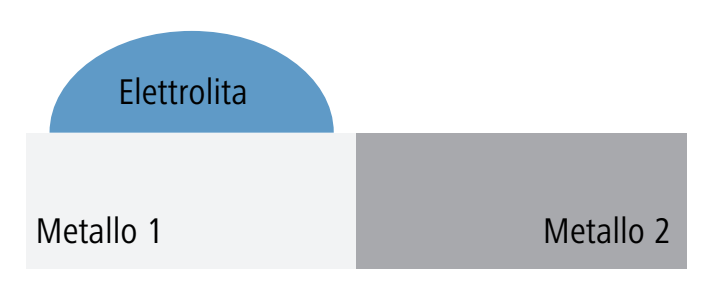
La struttura è realizzata in modo tale che un eventuale elettrolita possa entrare in contatto con un solo metallo. |
Evitare la corrosione bimetallica (fonte: Informationsstelle Edelstahl Rostfrei, Düsseldorf, foglio d’istruzioni 829).
3.5 Corrosione superficiale
La corrosione superficiale determina un’erosione superficiale che si verifica pressoché alla stessa velocità sull’intera superficie interessata del componente corroso. Le aree con erosione superficiale sono facilmente riconoscibili dalla decolorazione. La corrosione superficiale può comportare una significativa riduzione del peso del componente.
3.5.1 Immagine del danno
L’immagine del danno sotto riportata mostra la corrosione superficiale di un tubo in acciaio al carbonio. Il tubo è stato utilizzato in un impianto di acqua potabile. L’ossigeno presente nell’acqua potabile ha causato la corrosione da ossigeno, con conseguente erosione superficiale del metallo all’interno del tubo.
3.6 Corrosione per vaiolatura
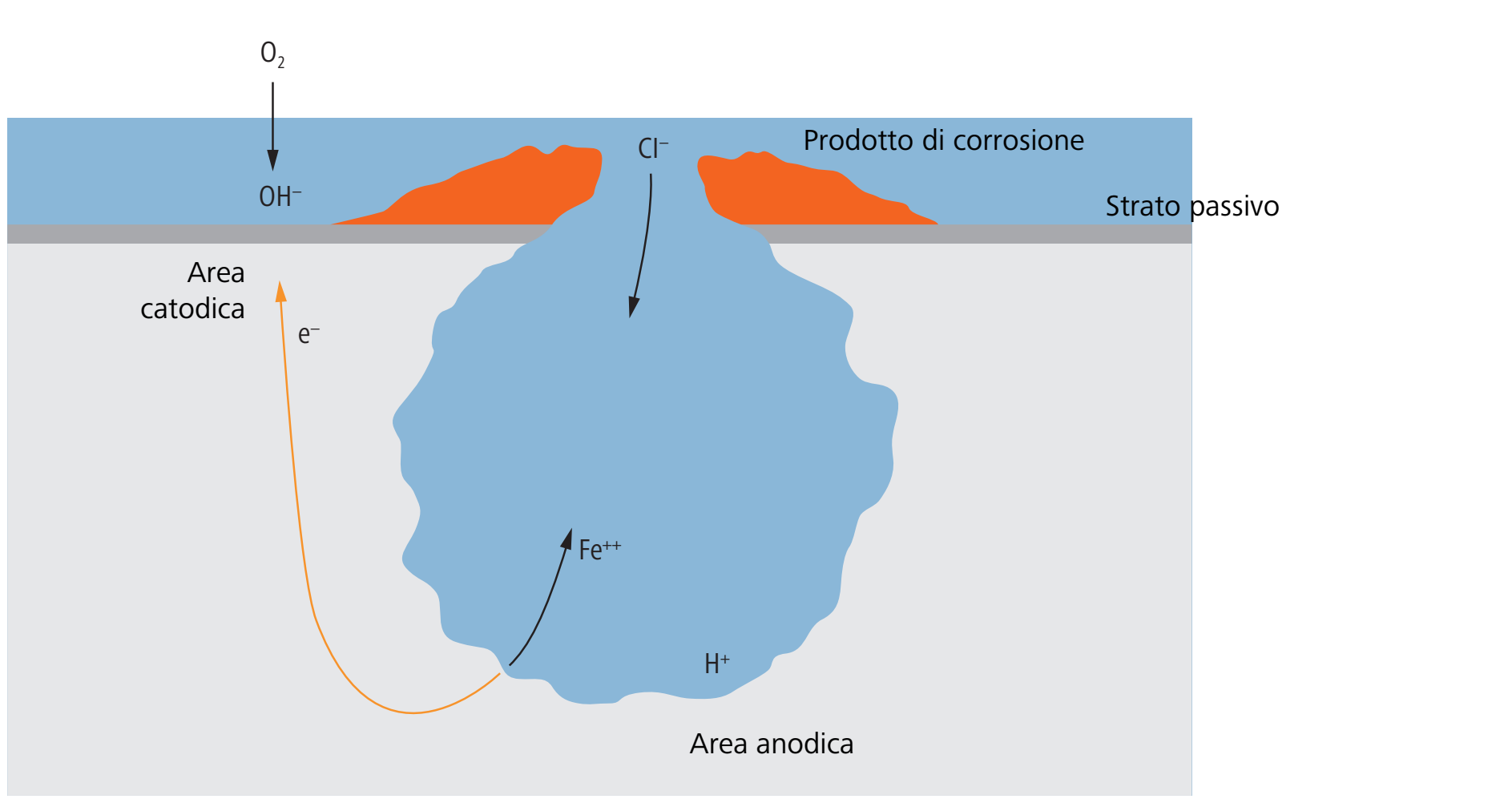
La corrosione per vaiolatura (perforazione) è una corrosione locale, spesso solo puntiforme, sul componente. Tra i punti con corrosione per vaiolatura possono esserci aree prive di corrosione. La corrosione per vaiolatura può estendersi fino a quando il componente interessato perde la sua funzione, ad esempio sotto forma di una crepa in una tubazione.
3.6.1 Corrosione per vaiolatura in acciai inossidabili (indice PRE)
La corrosione per vaiolatura in acciai inossidabili è causata principalmente da composti alogeni (composti di cloro, bromo e iodio). Come elemento di lega di acciai inossidabili, il molibdeno aumenta la resistenza alla corrosione per vaiolatura.
Il potenziale di corrosione per vaiolatura è una misura per la resistenza di un acciaio inossidabile alla corrosione per vaiolatura ed è espresso come somma effettiva o indice PRE (PRE: pitting resistance equivalent). Con il molibdeno come elemento di lega, la resistenza alla corrosione per vaiolatura può essere migliorata in modo mirato. L’indice PRE viene calcolato con la seguente formula:
Indice PRE = %Cr + 3.3 × %Mo
|
Simboli della formula |
Unità |
Descrizione |
|---|---|---|
|
Indice PRE |
— |
Potenziale di corrosione per vaiolatura |
|
%Cr |
Percentuale di lega del cromo |
|
|
%Mo |
Percentuale di lega del molibdeno |
Un indice PRE elevato indica unʼelevata resistenza alla corrosione per vaiolatura. I tipi di acciaio inossidabile utilizzati nei prodotti della
|
Tipi di acciaio inossidabile |
Indice PRE |
Indice PRE (valore normale) |
|---|---|---|
|
1.4521 |
24.1 |
23.0 |
|
1.4401/04 |
23.1 |
Indici PRE dei tipi di acciaio inossidabile della
3.6.2 Immagine del danno
La seguente immagine del danno mostra una corrosione per vaiolatura avanzata che ha causato la rottura di una tubazione.
3.6.3 Evitare la corrosione per vaiolatura
Per l’isolamento termico delle tubazioni occorre utilizzare materiali privi di alogeni.
Per impermeabilizzare i collegamenti filettati in acciaio inossidabile è necessario utilizzare canapa priva di cloro o altri sigillanti privi di cloruro. I sigillanti per filettature in materiale sintetico quali il politetrafluoroetilene (PTFE) devono essere certificati dal DVGW.
3.7 Tensocorrosione
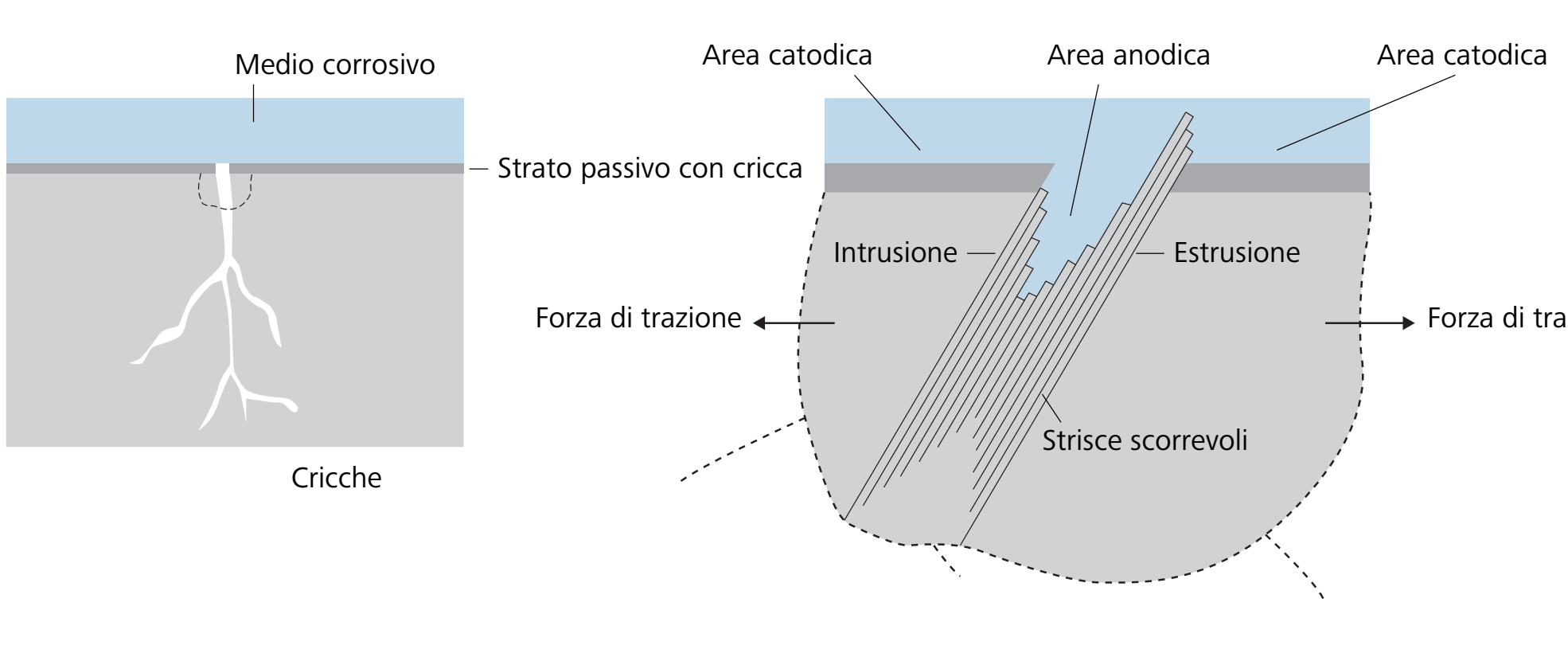
La tensocorrosione indica la fessurazione del metallo dovuta alla corrosione e all’allungamento del metallo per effetto delle sollecitazioni di trazione.
La tensocorrosione dei metalli, in particolare di acciai austenitici al Cr-Ni, è spesso causata da soluzioni saline contenenti cloruro o composti di cloro umidi. Le cricche sono spesso fortemente ramificate e si sviluppano perpendicolarmente alla direzione della sollecitazione di trazione sul componente. Questo tipo di corrosione si verifica piuttosto raramente negli acciai cromati ferritici.
La tensocorrosione può comparire nei fitting in ottone che vengono in contatto con ammoniaca o ammonio.
Le sollecitazioni di trazione necessarie per innescare la tensocorrosione possono essere presenti su un componente sotto forma di tensioni residue fin dall’inizio, come risultato del processo di produzione e lavorazione. Possono tuttavia essere causate anche da un montaggio conforme alle disposizioni o da sollecitazioni durante il funzionamento, ad esempio il prolungamento di un rubinetto è da considerarsi un’applicazione particolarmente critica da questo punto di vista poiché, in questo caso, vengono introdotte sollecitazioni di trazione a causa dell’espansione che si verifica durante l’avvitamento. I fattori determinanti in tal senso sono il grado di deformazione durante il montaggio e la durezza del componente che è una misura indiretta della deformabilità plastica. L’ottone deve essere sottoposto a stress termico per le applicazioni critiche. Oltre alle sollecitazioni meccaniche, la contemporanea esposizione a determinati agenti corrosivi specifici (ad esempio ammoniaca, ossido di zolfo) favorisce la tensocorrosione. Il bronzo è più resistente alla tensocorrosione rispetto all’ottone.
3.7.1 Immagini del danno
La seguente immagine del danno mostra la fase iniziale della tensocorrosione su un manicotto a scorrimento.
La seguente immagine del danno mostra un raccordo filettato in ottone da 1¼ × 1 pollici danneggiato da tensocorrosione.
3.8 Corrosione indotta dal flusso
La corrosione indotta dal flusso si riferisce ai processi di corrosione innescati dall’interazione tra il flusso di un medio e una superficie metallica. Comprende due forme: corrosione da erosione e corrosione per cavitazione. Entrambi i processi contrastano la formazione di strati superiori protettivi sulla superficie metallica, esponendo il materiale e favorendo la corrosione selettiva. Questo processo è particolarmente critico per rame e leghe di rame poiché la loro resistenza dipende dalla conformazione impeccabile di tali strati superiori.
3.8.1 Corrosione da erosione
La norma SN EN 12502-2:2004 descrive la corrosione da erosione come un tipo di corrosione caratterizzata da un’asportazione localizzata di materiale, spesso in combinazione con la corrosione chimica.
3.8.1.1 Erosione
Il processo fisico di erosione in sistemi di condutture si verifica quando l’acqua che scorre agisce meccanicamente sulla superficie della tubazione erodendola lentamente. Le cause più frequenti sono:
-
Elevate velocità di flusso: I flussi d’acqua veloci possono agire direttamente sulla parete del tubo ed eroderlo.
-
Particelle abrasive: Le particelle trasportate dall’acqua, quali sabbia o altre sostanze solide, possono danneggiare la parete interna del tubo per attrito.
-
Flussi turbolenti: I bruschi cambiamenti nella direzione del flusso o i restringimenti nel sistema di tubazioni possono comportare flussi turbolenti che accelerano l’asportazione di materiale.
L’erosione determina una graduale perdita di materiale che riduce lo spessore delle pareti dei tubi e può comprometterne l’integrità strutturale.
3.8.1.2 Conseguenze
-
Lo strato superiore viene danneggiato o la sua formazione viene contrastata, ad esempio lo strato protettivo di ossido o carbonato sulle superfici in rame.
-
La superficie metallica esposta dallo strato superiore è soggetta a una maggiore corrosione chimica perché lo scambio di ioni non è più inibito.
-
La corrosione locale si manifesta con i caratteristici avvallamenti a forma di ferro di cavallo.
-
Nei sistemi di approvvigionamento di acqua calda, la corrosione da erosione si verifica spesso in punti in cui la direzione di flusso cambia bruscamente, ad esempio sugli spigoli.
3.8.1.3 Prevenzione
La norma EN 12502-2 contiene raccomandazioni sulle velocità massime di flusso e sull’esecuzione di tubazioni. Le specifiche devono essere intese come valori indicativi e servono come ausilio per la progettazione e il funzionamento di tubazioni con acqua come medio.
Osservanza dei valori limite per le velocità di flusso.
-
Tubazioni in rame:
-
Con tempi di prelievo brevi: max. 3 m/s
-
Con tempi di prelievo prolungati (> 15 minuti): max. 2 m/s
-
In sistemi di circolazione per approvvigionamento di acqua calda: max. 0.5 m/s
-
-
Per tubazioni in leghe di rame valgono gli stessi valori limite delle tubazioni in rame. In presenza di una maggiore resistenza alla corrosione sono tuttavia possibili velocità di flusso più elevate.
-
Tubazioni in bronzo: in sistemi di circolazione per approvvigionamento di acqua calda: max. 1 m/s tenendo conto della qualità dell’acqua e dell’esecuzione delle tubazioni
Prevenire turbolenze nelle tubazioni:
-
Evitare bruschi cambiamenti di sezione e di direzione nelle tubazioni.
-
Utilizzare elementi di compensazione del flusso, ad esempio un tratto di tubo diritto a valle di una pompa di circolazione.
-
Ridurre al minimo il numero tubi curvati e valvole nella rete di tubazioni.
Selezione dei materiali:
-
Se non è possibile rispettare le velocità di flusso raccomandate dalla norma EN 12502-2 è opportuno utilizzare acciaio inossidabile al posto del rame e delle leghe di rame. L’acciaio inossidabile vanta una maggiore resistenza alla corrosione ed è più adatto a fronte di condizioni di flusso critiche.
-
Se è possibile rispettare le specifiche della norma EN 12502-2 si dovrebbero utilizzare leghe di rame con una maggiore resistenza all’erosione. Al posto dell’ottone si dovrebbe utilizzare il bronzo che presenta una maggiore resistenza alla corrosione da erosione.
3.8.1.4 Immagine del danno
La seguente immagine del danno mostra la corrosione da erosione su una valvola inclinata installata in una conduttura di circolazione. A causa di un blocco meccanico del pezzo per valvola di ritegno (non raffigurato), la potenza della pompa di circolazione è stata aumentata per mantenere la portata volumetrica nella conduttura di circolazione. Ciò ha comportato velocità di flusso elevate e flussi turbolenti nell’area del piattello nonché, di conseguenza, una corrosione da erosione.
3.8.2 Corrosione per cavitazione
La corrosione per cavitazione è causata dalla cavitazione che danneggia meccanicamente la superficie metallica e favorisce quindi la corrosione chimica.
3.8.2.1 Cavitazione
Il processo fisico della cavitazione si verifica quando differenze di pressione locali nel liquido portano alla formazione e al successivo collasso di bolle di gas. Le cause della cavitazione nelle tubazioni sono:
-
Variazioni di pressione: In aree con velocità di flusso elevate o in corrispondenza di strozzature, la pressione può diminuire, a livello locale, a tal punto che l’acqua evapora e forma bolle di gas.
-
Implosione delle bolle: Quando queste bolle raggiungono aree con una pressione maggiore implodono. I sovraccarichi che ne derivano possono danneggiare la parete del tubo.
-
Azione ripetuta: Il collasso ripetuto delle bolle può comportare un’asportazione progressiva del materiale, nota come «erosione per cavitazione».
La cavitazione provoca danni localizzati che spesso si manifestano come piccoli avvallamenti o fori nella parete del tubo. Tali danni possono espandersi e compromettere il funzionamento della tubazione.
3.8.2.2 Conseguenze
-
La corrosione per cavitazione si verifica tipicamente in pompe, valvole o strozzature con marcate differenze di pressione.
-
Danneggiamento del materiale con avvallamenti a forma di vescicola.
-
In particolare nelle leghe di rame:
-
Lo strato superiore, ad esempio il carbonato di rame basico, viene danneggiato dalla cavitazione.
-
Il metallo esposto è soggetto a corrosione selettiva, soprattutto in acque acide o contenenti solfati.
-
3.8.2.3 Prevenzione
Le condizioni di flusso e la qualità dell’acqua rappresentano i fattori critici che possono innescare la corrosione per cavitazione:
-
Evitare velocità di flusso eccessive e variazioni di pressione improvvise, ad esempio in corrispondenza di pompe e punti di strozzamento.
-
Evitare l’acqua sovrasatura di gas perché favorisce la formazione di bolle di gas, ad esempio a causa di uno sfiato incontrollato delle tubazioni.
-
In particolare nelle tubazioni in rame e leghe di rame:
-
Ridurre la formazione di bolle di gas utilizzando dispositivi di sfiato.
-
Evitare perdite di pressione dimensionando adeguatamente le tubazioni e le pompe.
-
3.8.2.4 Immagini del danno
L’immagine seguente mostra la corrosione per cavitazione generata in condizioni di laboratorio su una piastra di prova in bronzo privo di piombo. La piastra di prova e un sonotrodo a ultrasuoni sono stati collocati in un recipiente pieno di acqua. La piastra di prova è stata quindi trattata con il sonotrodo a ultrasuoni per un determinato lasso di tempo. Il trattamento con ultrasuoni ha causato una cavitazione che ha portato a un’asportazione di materiale visibile sulla superficie della piastra di prova.
La seguente immagine del danno mostra una forma mista di corrosione da erosione e di corrosione per cavitazione su un riduttore di pressione.
3.9 Corrosione selettiva
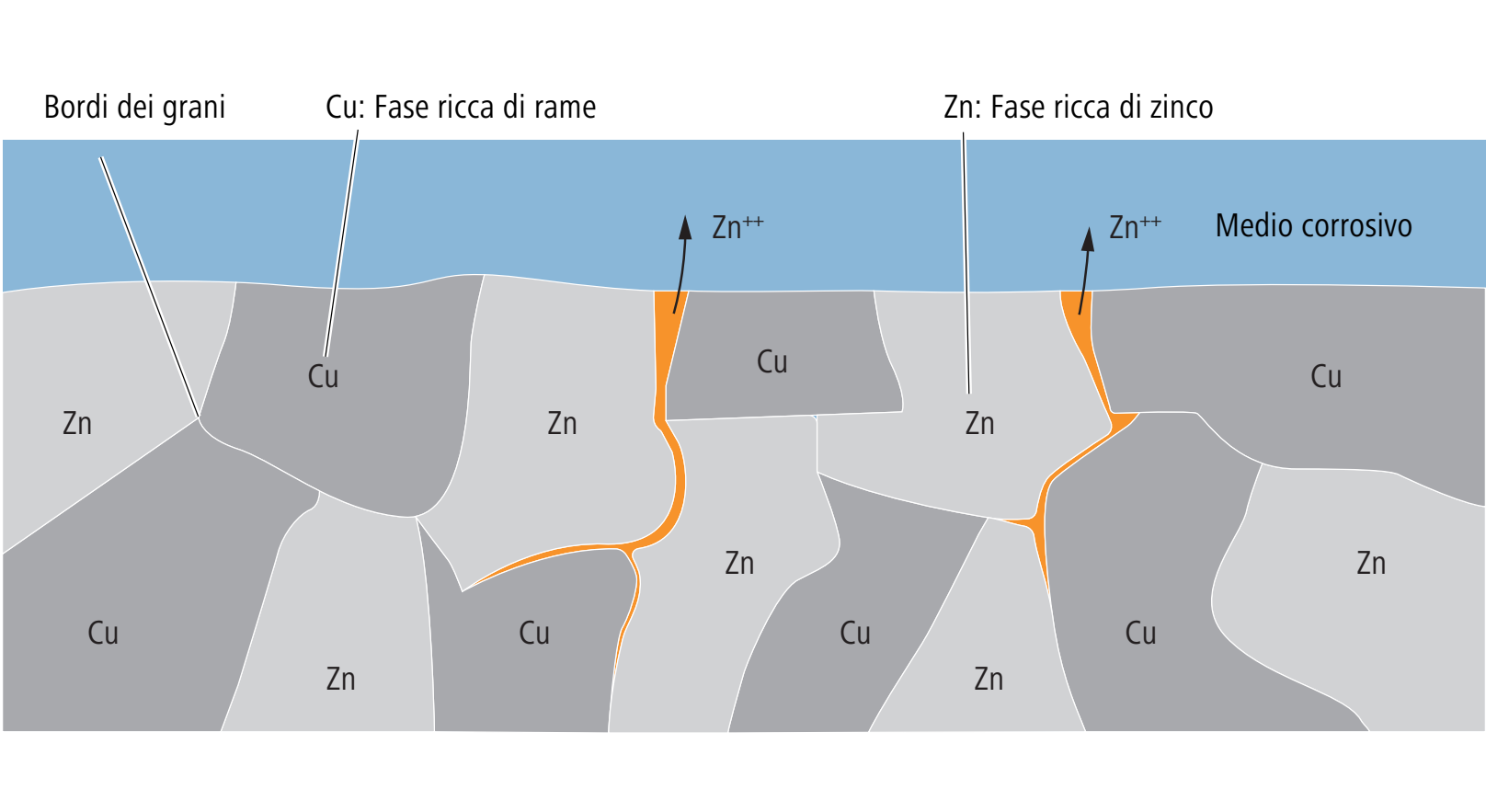
La corrosione selettiva è la corrosione di una lega in cui gli elementi formano un elemento di corrosione a causa dei diversi potenziali elettrochimici, con l’acqua che in molti casi costituisce l’elettrolita. L’elemento della lega meno nobile si corrode lungo le aree strutturali del materiale. L’elemento più nobile della lega permane nel materiale in uno stato poroso. Un esempio di corrosione selettiva è rappresentato dalla dezincificazione dell’ottone.
3.9.1 Dezincificazione
Un esempio di corrosione selettiva è la dezincificazione di componenti di condutture in ottone. Nella dezincificazione, lo zinco viene dissolto dalla lega di ottone per corrosione, lasciando il rame poroso. Le croste di sale sulla parte esterna delle rubinetterie in ottone indicano una possibile dezincificazione che può verificarsi soprattutto nelle condutture dell’acqua calda.
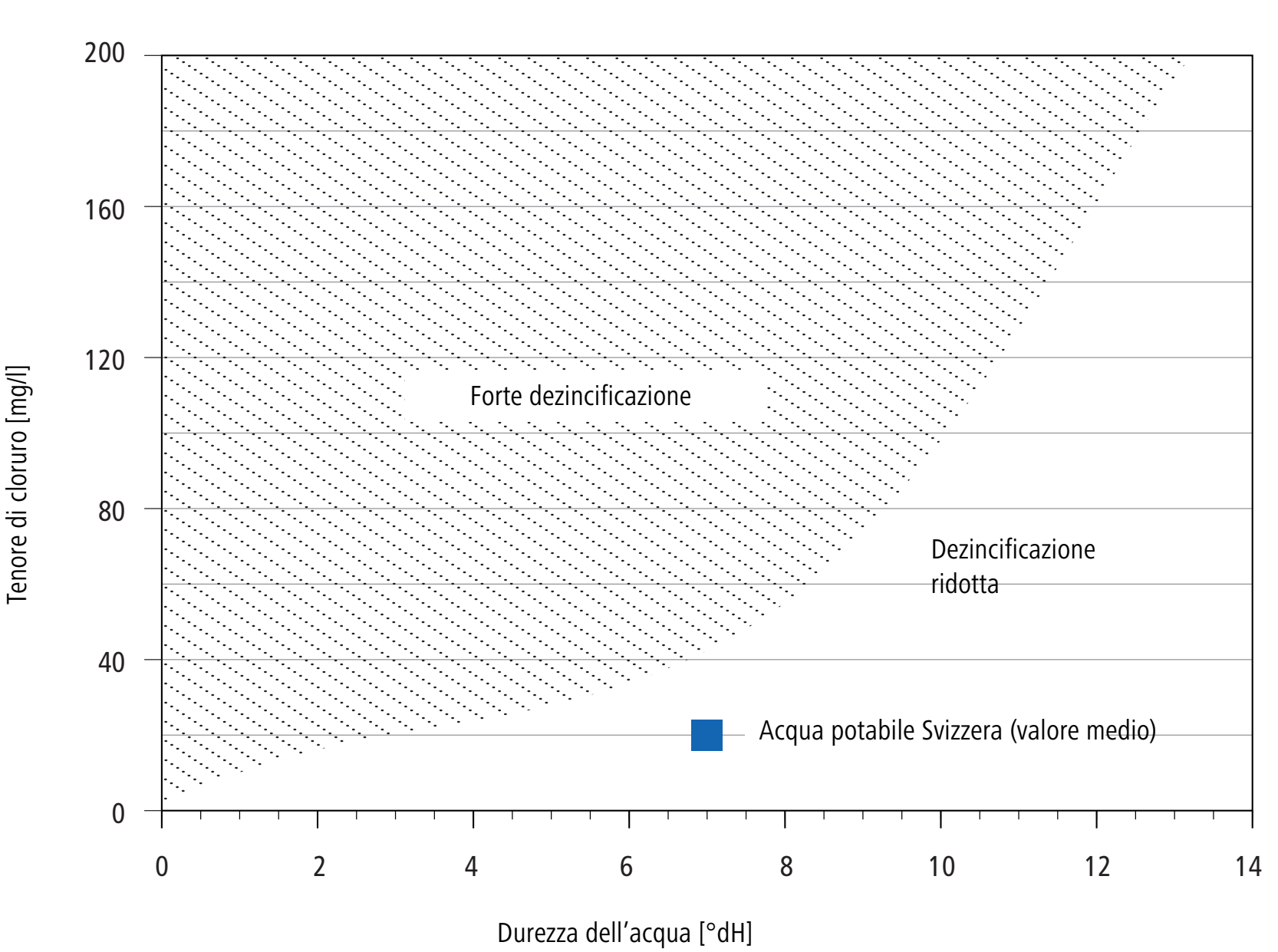
3.9.2 Diagramma di Turner
La composizione dell’acqua influisce sulla dezincificazione dell’ottone. Una maggiore durezza dell’acqua e un minore tenore di cloruro ostacolano la dezincificazione. La correlazione tra dezincificazione, durezza dell’acqua e tenore di cloruro è riscontrabile nel diagramma di Turner.
3.9.3 Immagine del danno
La seguente immagine del danno mostra la dezincificazione sul filetto di una testa della valvola. La resistenza del componente è stata ridotta dalla progressiva dezincificazione a tal punto che il componente non riusciva più a sopportare le forze del raccordo.
3.10 Corrosione intercristallina
La corrosione intercristallina è la corrosione all’interno o adiacente ai bordi dei grani di una lega metallica.
La corrosione intercristallina viene favorita da una struttura a grana grossa e da elevate proporzioni degli elementi di lega arsenico e fosforo nel materiale nonché da temperature elevate. Anche l’ammoniaca presente nell’acqua e negli elementi di sfiato può causare la corrosione intercristallina.
Nelle leghe di ottone, la corrosione intercristallina si verifica quando sono presenti precipitati ai bordi dei grani. La dezincificazione dell’ottone è dovuta sia alla corrosione per vaiolatura sia alla corrosione intercristallina.
3.10.1 Immagine del danno
La seguente immagine del danno mostra la corrosione intercristallina su un componente in ottone.
Se sul componente agiscono sollecitazioni di trazione meccaniche, in combinazione con la corrosione intercristallina possono verificarsi cricche da stress, come risulta nell’immagine seguente:
3.11 Corrosione per correnti esterne
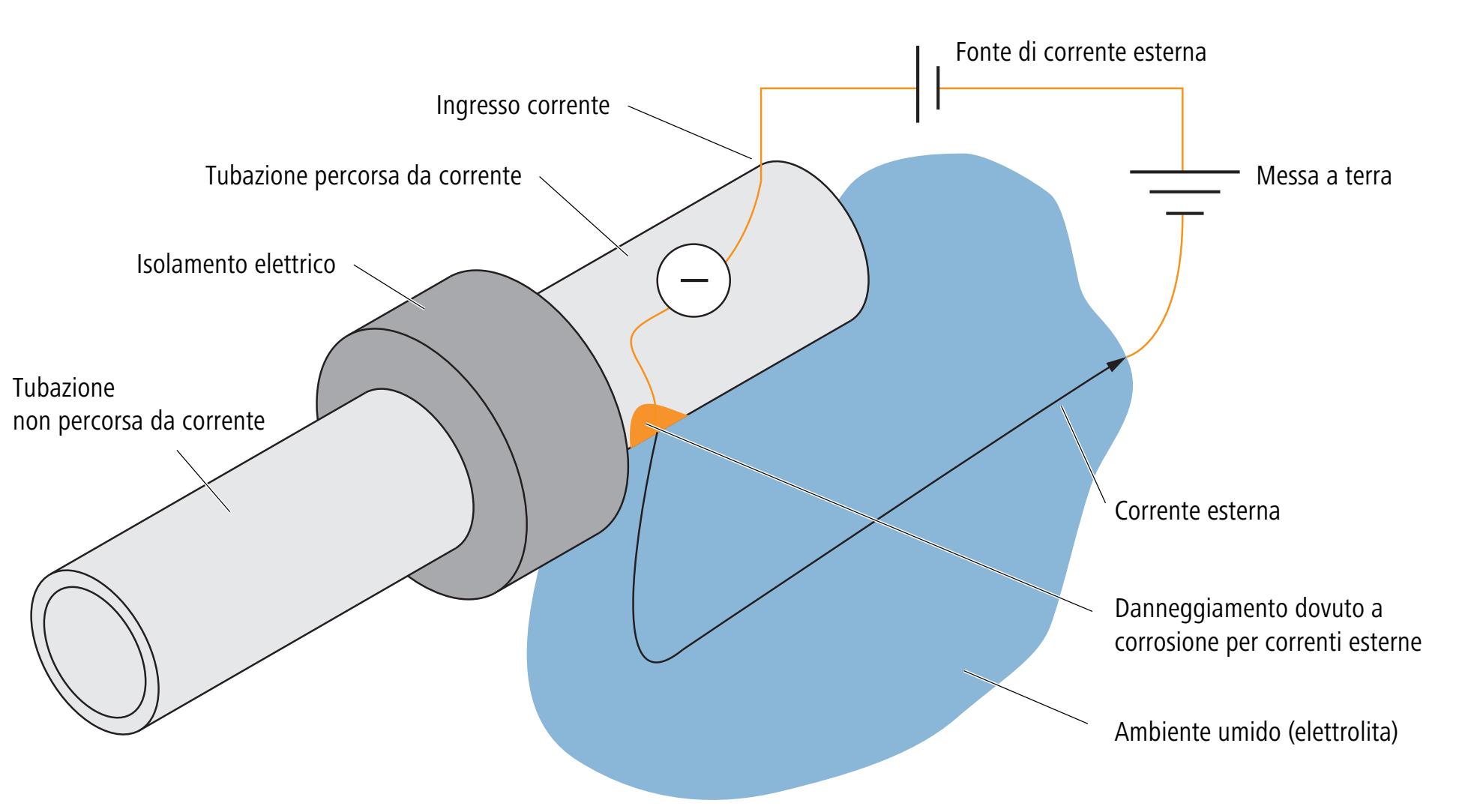
La corrosione per correnti esterne è una corrosione elettrochimica dovuta a correnti appunto esterne (denominate anche «correnti vaganti» o «correnti vagabonde») che possono verificarsi quando le correnti elettriche vengono condotte nel terreno attraverso una messa a terra e vengono deviate con isolamenti e resistenze. Queste possono essere correnti continue o alternate – ma solo le correnti continue sono rilevanti come causa di corrosione.
Se una corrente continua attraversa una parte metallica in un ambiente umido si può innescare una reazione anodica parziale del metallo con l’ossigeno – e la parte metallica si corrode.
L’isolamento elettrico nell’immagine serve a mostrare la deviazione della corrente esterna dalla tubazione in un ambiente a bassa impedenza dove successivamente si può verificare la corrosione dei punti di uscita.
3.11.1 Evitare la corrosione per correnti esterne
Una possibile causa di corrosione per correnti esterne nell’impianto idrosanitario è rappresentata dagli allacciamenti elettrici dell’abitazione. A seconda del sistema di rete e delle utenze, le correnti esterne possono verificarsi nelle tubazioni, negli impianti di ventilazione e di riscaldamento, negli impianti parafulmine e negli elementi metallici della struttura. In presenza di umidità possono manifestarsi fenomeni di corrosione.
Nei sistemi di rete TN, i conduttori attivi della rete elettrica sono collegati al potenziale di terra attraverso il punto stella del trasformatore, mentre le utenze elettriche sono collegate a questo punto in due modi diversi:
-
Nella rete TN-C (dal francese «terre neutre combiné»), il collegamento avviene tramite il conduttore PEN che combina la funzione del conduttore di protezione (PE) e del conduttore di neutro (N).
-
Nella rete TN-S (dal francese «terre neutre séparé»), il conduttore di neutro e il conduttore di protezione sono posati separatamente.
La combinazione dei due sistemi di rete è denominata rete TN-C-S.
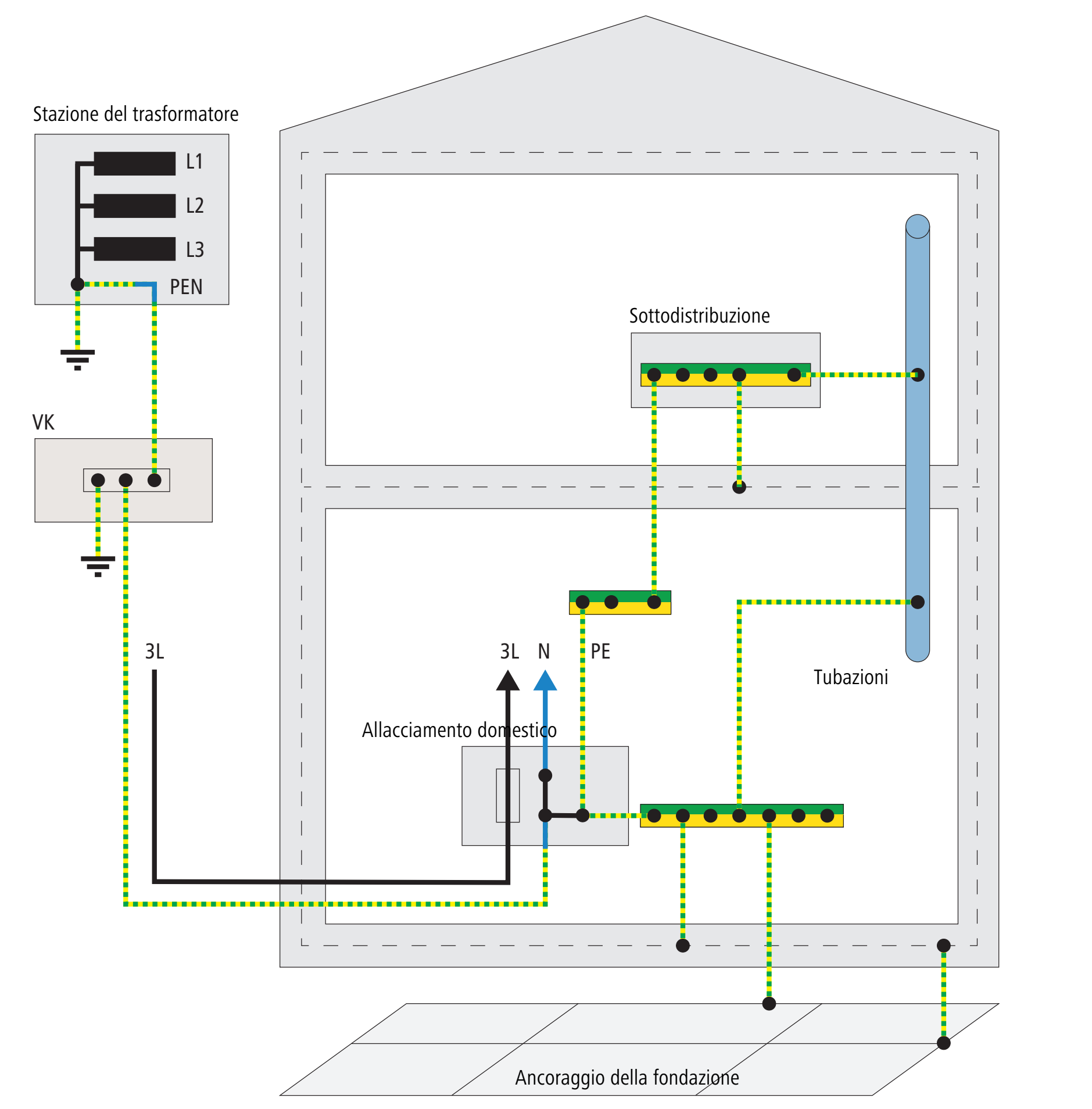
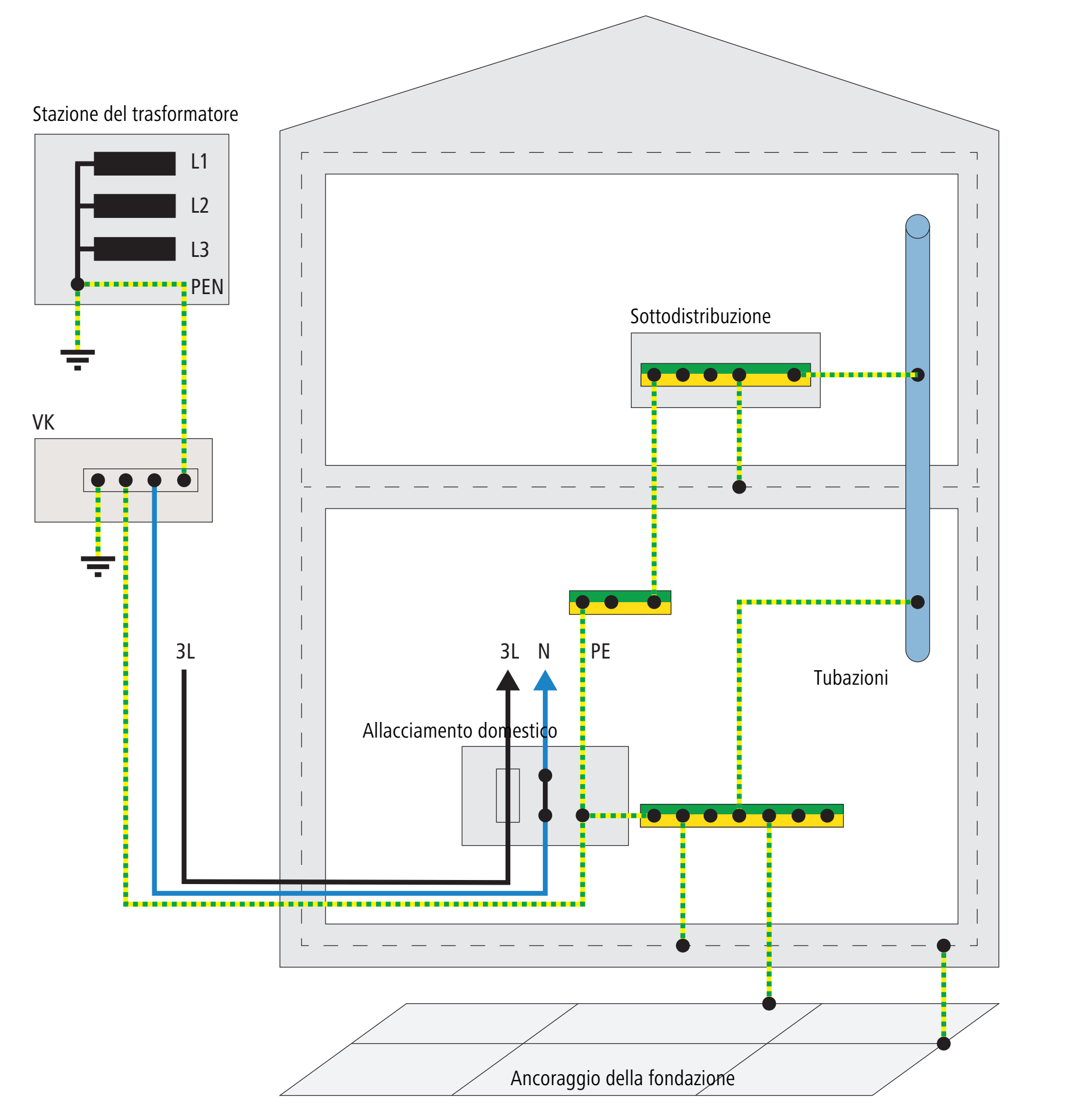
3.11.1.1 Sistema di rete TN-C
Il sistema TN-C prevede un conduttore PEN comune nei collegamenti tra la scatola dell’allacciamento domestico e le sottodistribuzioni. Un conduttore di protezione (PE) separato è spesso presente solo nel circuito elettrico verso l’utenza.
3.11.1.2 Sistema di rete TN-S
Il sistema di rete TN-S prevede la suddivisione del conduttore PEN in conduttore di protezione e conduttore di neutro, creata in corrispondenza dell’allacciamento elettrico dell’abitazione.
3.11.1.3 Messa a terra di impianti elettrici
La messa a terra di impianti elettrici allʼinterno di edifici è costituita da un dispositivo di protezione elettrica che, in caso di guasto, blocca l’alimentazione di tensione a parti prive di corrente.
La messa a terra attraverso la rete di approvvigionamento di acqua potabile è sconsigliata per i seguenti motivi:
-
Le correnti esterne provenienti da impianti elettrici possono attraversare la rete di approvvigionamento di acqua potabile e causare corrosione per correnti esterne.
-
In caso di sostituzione o riparazione di tubazioni (metalliche), la messa a terra può essere interrotta.
Quando si effettua la messa a terra attraverso l’allacciamento domestico dell’acqua, la fonte di corrente esterna può trovarsi lontano dall’edificio. Ciò può complicare notevolmente lʼindividuazione di fonti di correnti esterne per impedire che si verifichino. Occorre inoltre tener conto del fatto che il numero di fonti di correnti esterne è in aumento a causa del crescente utilizzo di dispositivi elettrici, con utenze non lineari che diventano sempre più importanti come fonti di interferenza.
In alternativa si può effettuare la messa a terra con:
-
Dispersori di terra nelle fondazioni
-
Nastri di messa a terra
-
Picchetti di terra o dispersori di profondità
-
Altri elementi costruttivi conficcati nel terreno
|
1 |
Raccordo per l’acqua all’abitazione |
|
2 |
Dispersore di terra nella fondazione (parte dell’armatura del muro) |
|
3 |
Conduttore di protezione di impianti elettrici |
|
4 |
Nastro di messa a terra |
|
5 |
Cavo o ponticello a filo |
La messa a terra di impianti elettrici deve essere effettuata e verificata da elettricisti specializzati.
3.12 Biocorrosione (MIC)
La biocorrosione, nota anche come corrosione influenzata microbiologicamente» (abbreviata in MIC per «microbial influenced corrosion»), è un processo in cui i microrganismi accelerano la corrosione di metalli. I ferrobatteri e i batteri solfato-riduttori svolgono un ruolo importante in questo processo.
-
I ferrobatteri (abbreviati in IRB per «iron relevant bacteria») sono microrganismi aerobi che utilizzano gli ossidi di ferro come fonte di energia. I ferrobatteri ossidano il ferro divalente (Fe²⁺) in ferro trivalente (Fe³⁺) con conseguente formazione di depositi di ossido di ferro e idrossido che possono ricoprire la superficie dei metalli e accelerare la corrosione.
-
I batteri solfato-riduttori (abbreviati in SRB per «sulfat reducing bacteria») sono microrganismi anaerobi che riducono il solfato (SO₄²-) in solfuro (S²-). Il solfuro formatosi può reagire con il ferro e formare solfuro di ferro che crea sulla superficie metallica uno strato nero e fangoso. Tale strato può favorire ulteriormente la corrosione.
A differenza di altri tipi di corrosione, la biocorrosione è indipendente dalla concentrazione di ossigeno. I batteri solfato-riduttori proliferano in ambienti poveri di ossigeno, mentre i ferrobatteri sono attivi in presenza di ossigeno. Per questo motivo, la biocorrosione può verificarsi in ambienti ricchi e poveri di ossigeno.
3.12.1 Forme
La biocorrosione può assumere varie forme, a seconda dei microrganismi coinvolti:
-
I ferrobatteri formano sulla superficie metallica depositi color ruggine o marroni.
-
I batteri solfato-riduttori formano depositi neri e fangosi che possono odorare di uova marce (a causa della formazione di idrogeno solforato).
3.12.2 Biocorrosione in impianti sprinkler
In impianti sprinkler, la biocorrosione può causare difetti di tenuta nelle tubazioni e, di conseguenza, malfunzionamenti. Il ristagno dell’acqua in impianti sprinkler favorisce la crescita di microrganismi, soprattutto se l’impianto sprinkler viene attivato di rado. I tubi in ferro zincato sono particolarmente soggetti alla biocorrosione perché lo strato di zinco viene attaccato dall’attività dei batteri solfato-riduttori e dei ferrobatteri. L’utilizzo di acciaio inossidabile può ridurre significativamente la biocorrosione negli impianti sprinkler.
3.12.3 Immagini del danno
La seguente immagine del danno mostra la biocorrosione causata da ferrobatteri (IRB) all’interno di un tubo in acciaio al carbonio non zincato. Dopo aver smontato il tubo, l’area a sinistra della linea blu è stata pulita, mentre l’area a destra è stata lasciata inalterata.
La seguente immagine del danno mostra la biocorrosione causata da batteri solfato-riduttori (SRB) su un elemento in rame del quadro elettrico.