Thématiques - Corrosion
261.0.053 / V8
3 Types de corrosion
Dans toute corrosion électrolytique, le processus anodique correspond toujours à une dissolution du métal (oxydation). Le processus cathodique (réduction) peut par contre être formé par diverses réactions. Le type de corrosion est souvent dénommé d’après la réduction ou l’oxydant.
3.1 Corrosion à haute température
La corrosion des métaux à haute température se produit en association avec des gaz secs, sans l’action d’un électrolyte. Les réactions d’oxydation et de réduction correspondantes se produisent à des températures de 400 °C et supérieures.
Lors de l’oxydation de métaux avec des gaz tels que l’oxygène, il se forme à leurs surfaces des couches d’oxydes métalliques plus ou moins stables. Pour la corrosion à haute température, on peut citer comme exemple le calaminage des surfaces métalliques durant l’usinage du métal.
Comme tous les cas de corrosion sont dûs à l’origine à une action électrochimique, la corrosion à haute température n’est pas traitée plus en détail dans le présent document.
3.2 Corrosion par oxygène
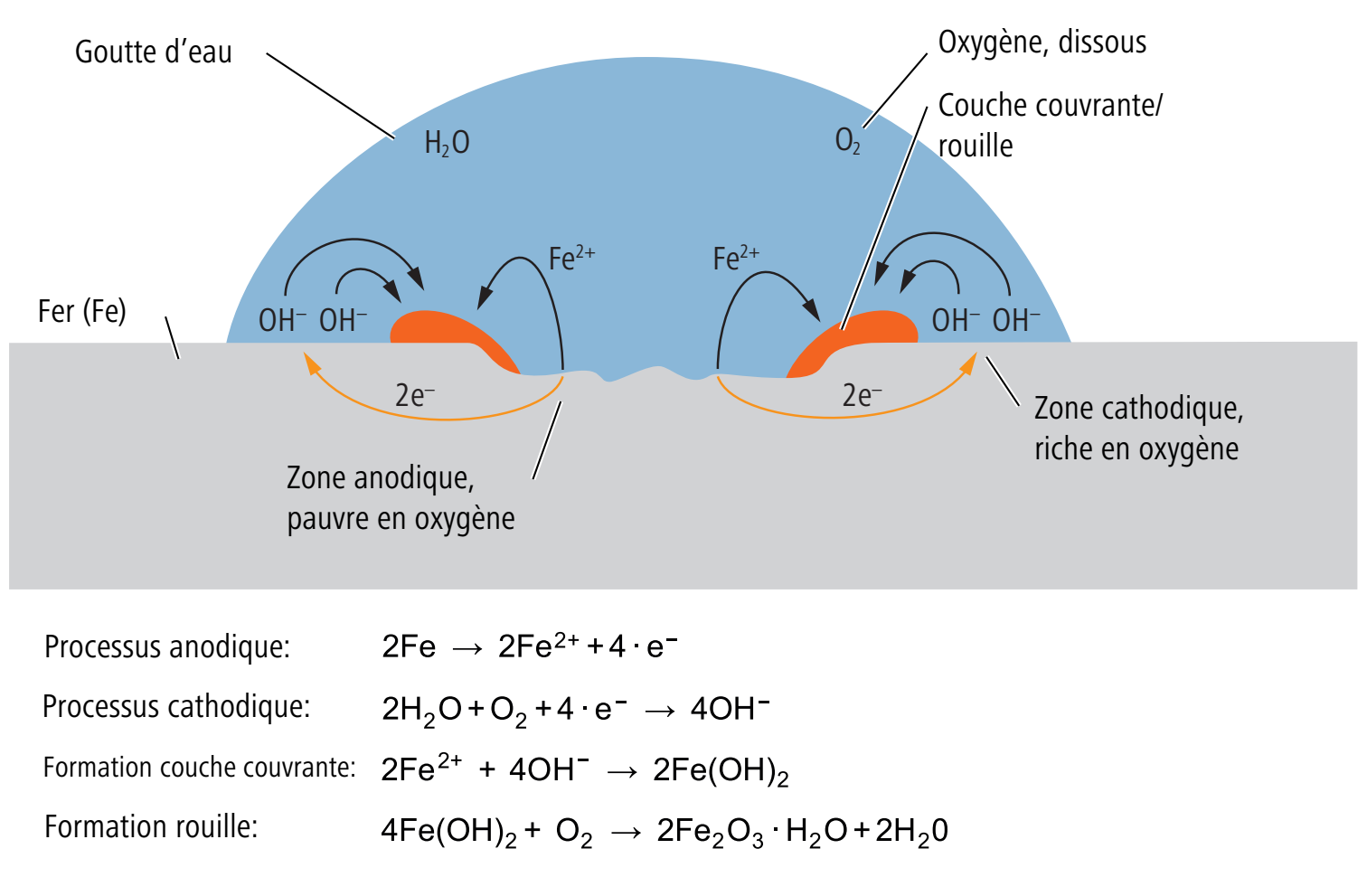
En raison de la présence d’oxygène dans l’air et de son potentiel aux valeurs toujours fortement positives, la corrosion par oxygène est la plus fréquente parmi les types de corrosion. Lors de la corrosion par oxygène, le processus cathodique induit une réduction de l’oxygène en ions oxygène. La corrosion par oxygène se produit déjà à différentes concentrations d’électrolyte qui forment une cellule de concentration, p. ex. dans une goutte d’eau sur une surface en fer.
Il s’ensuit que le processus cathodique se déroule en périphérie de la goutte d’eau, là où la concentration d’oxygène est plus élevée. Dans la partie centrale s’opère la dissolution du métal (processus anodique), qui déclenche d’autres réactions se traduisant par la formation de rouille.
La corrosion par oxygène se produit surtout dans des électrolytes neutres ou alcalins à valeur pH >7. En présence d’électrolytes acides (valeur pH <7), l’hydrogène prédomine dans l’électrolyte, et la corrosion ne se fait plus par oxygène mais par hydrogène. Tous les métaux dont le potentiel est inférieur à celui de l’oxygène peuvent être attaqués par la corrosion par oxygène.
3.3 Corrosion par hydrogène
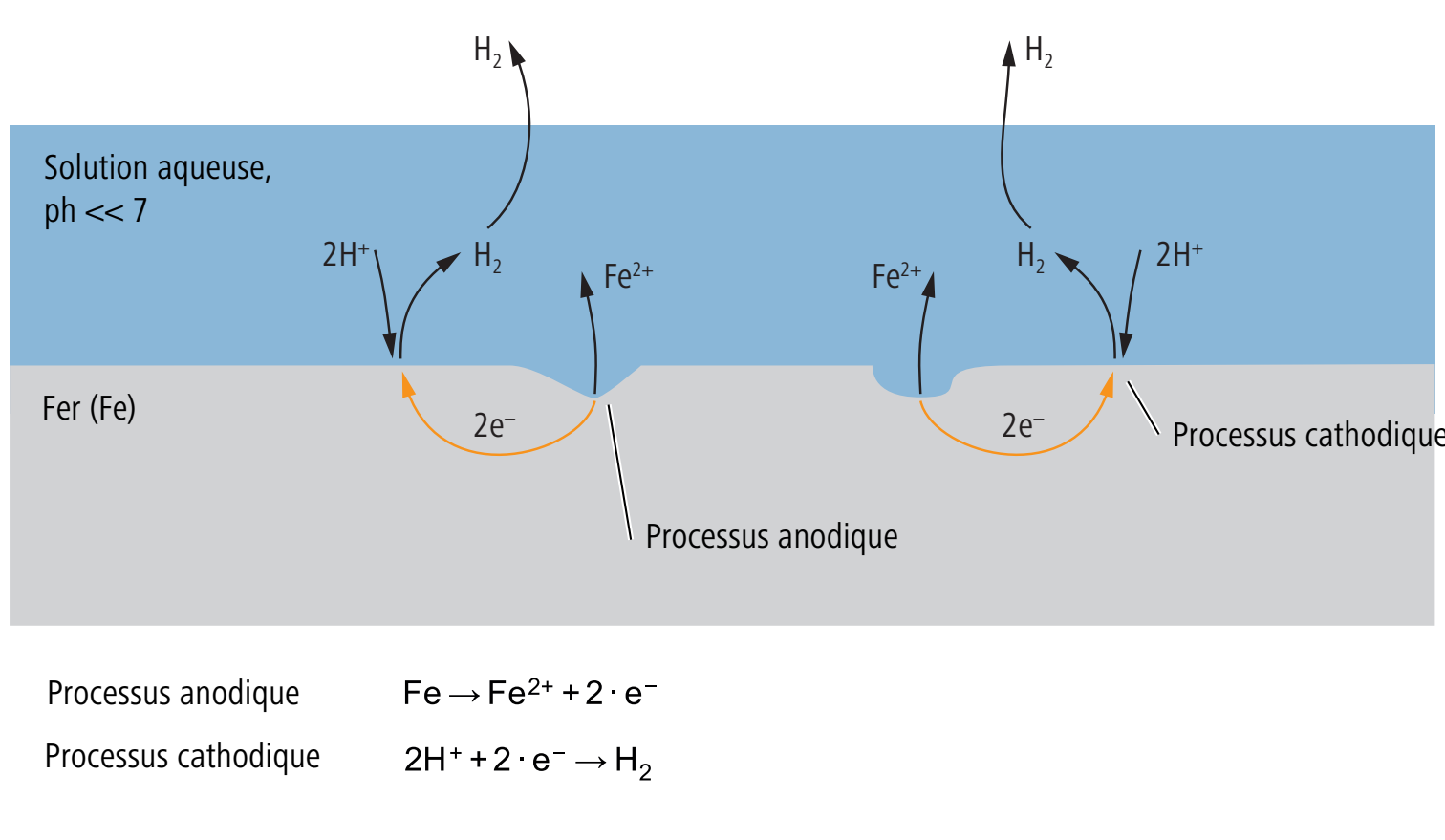
La corrosion par hydrogène survient dans des solutions fortement acides, même en l’absence totale d’oxygène. Ces solutions ont des valeurs pH faibles et présentent par conséquent des concentrations élevées en hydrogène.
Lors d’une corrosion par hydrogène, le processus cathodique correspond à une réduction d’ions d’hydrogène H+ en hydrogène gazeux H2. Comme pour tous les types de corrosion, le processus anodique correspond à la dissolution du métal par la libération d’électrons qui se détachent du réseau métallique et par la formation d’ions métalliques. Le processus anodique et cathodique s’opère sur toute la surface métallique, à des endroits et moments différents. Dans le cas d’une corrosion par hydrogène, il n’est pas possible de localiser l’anode et la cathode.
Pour les métaux non-nobles, il a été établi que, dans des solutions aqueuses et fortement acides, ils sont exposés aussi bien à la corrosion par hydrogène que par oxygène. Les métaux nobles par contre ne connaissent que la corrosion par hydrogène dans des solutions aqueuses à faibles valeurs pH. Ceci confirme l’expérience selon laquelle les acides ont une action plus agressive que les solutions alcalines.
3.4 Corrosion bimétallique
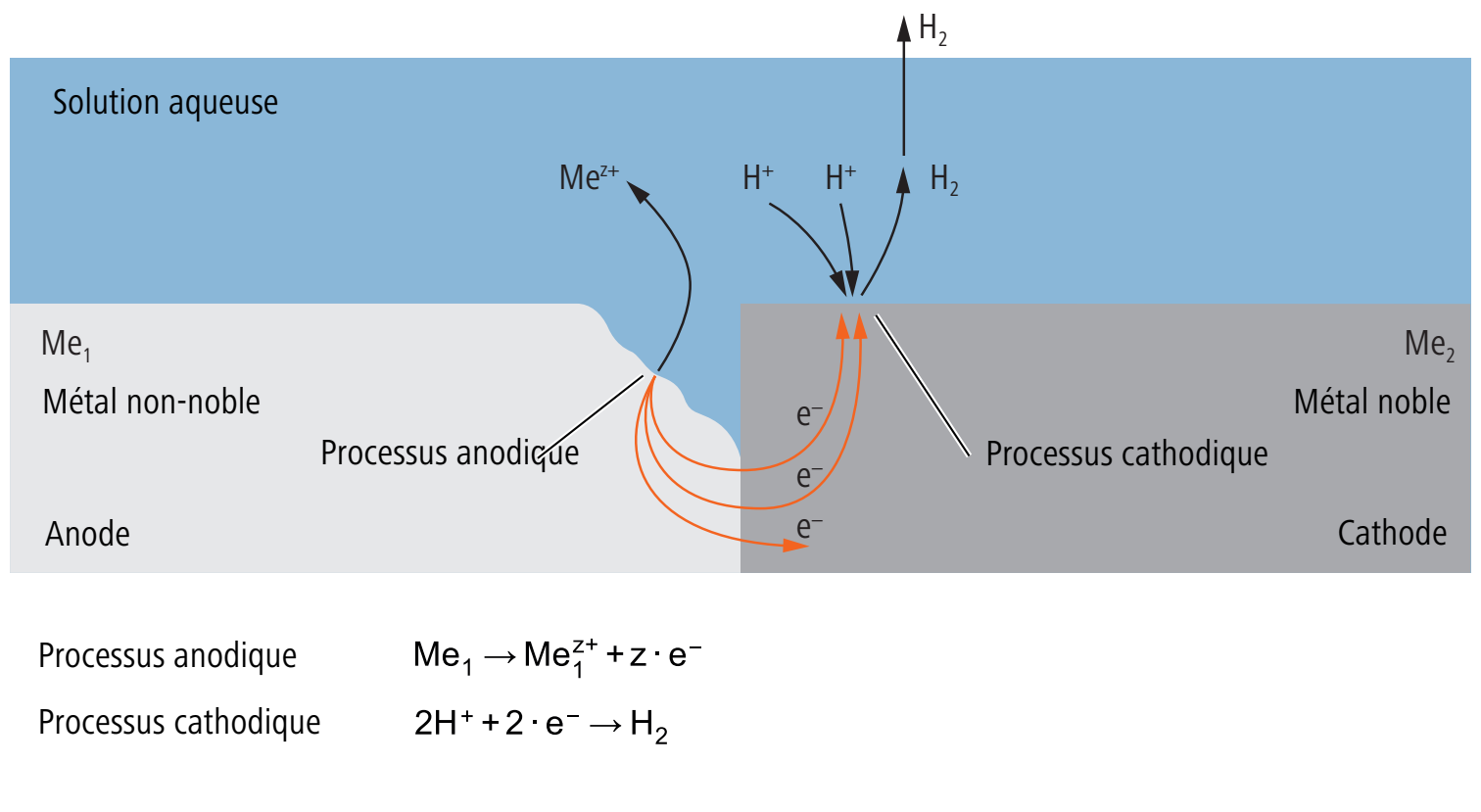
On assiste à une corrosion bimétallique lorsque des métaux à potentiel électrochimique différent forment un élément galvanique court-circuité, le métal le moins noble faisant l’objet d’une attaque corrosive.
La photo montre comme processus cathodique la réduction par hydrogène, une réduction par oxygène étant cependant aussi possible.
Les paramètres suivants renforcent la corrosion bimétallique:
-
Différence de potentiel élevée des métaux
-
Conductibilité élevée des métaux et de l’électrolyte
-
Conductibilité élevée des surfaces de contact entre les métaux
On peut en déduire des mesures pour réduire la corrosion bimétallique, p. ex. en évitant les installations mixtes ou l’isolation électrique des métaux.
Dans une installation d’eau de boisson se crée un éIément de corrosion aux points de contact pour les raisons suivantes: contact métallique d’éléments de conduites de différents matériaux métalliques et de l’eau de boisson et/ou de l’eau de condensation agissant comme électrolyte. On assiste à la circulation d’un courant de corrosion.
3.4.1 Aspect des dommages
La photo ci-dessous montre les dommages que la corrosion bimétallique a causés sur une conduite. La corrosion bimétallique a été provoquée par des colliers inadéquats.
La photo suivante montre la corrosion bimétallique sur un raccord dans des conditions de laboratoire. Cette corrosion a été provoquée par la combinaison de deux matériaux, à savoir d’un tuyau en acier inox et d’un raccord en acier C. Sur la photo, la corrosion bimétallique n’est pas directement visible. On voit juste les produits de corrosion sous forme de dépôts blanchâtres.
3.4.2 Comment éviter la corrosion bimétallique
Il existe diverses mesures pour éviter la corrosion bimétallique. D’une part en minimisant la différence de potentiel électrochimique des matériaux et, d’autre part, en évitant l’apparition de courants de corrosion.
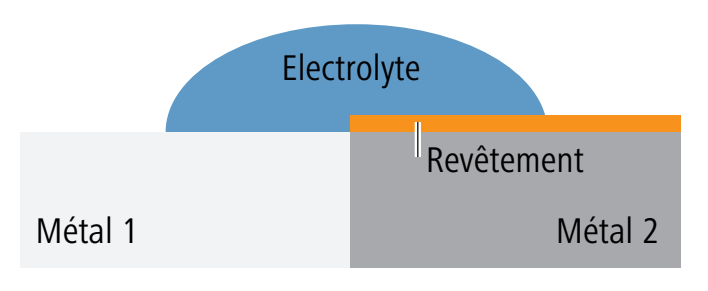
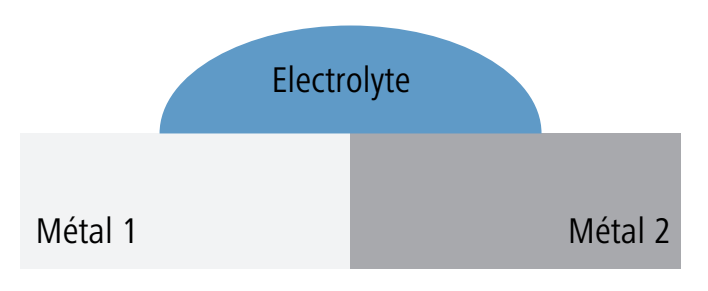
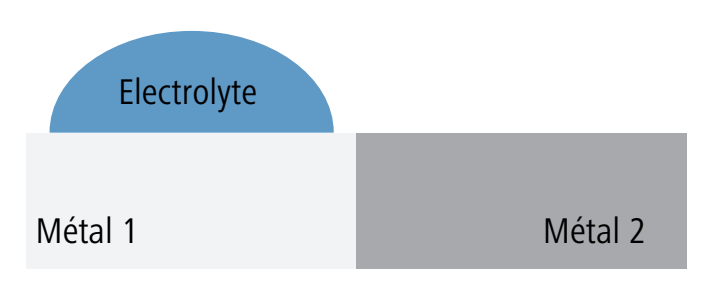
Les schémas du tableau suivant montrent les diverses mesures permettant d’éviter la corrosion bimétallique:
|
Photo |
Description |
|---|---|
|
|
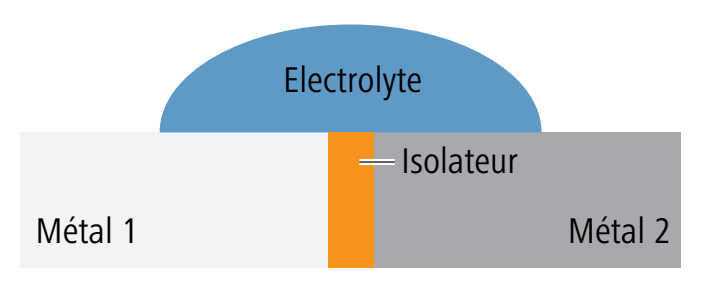
Le courant de corrosion est empêché par un élément d’isolation électrique, p. ex. une douille à collerette 90056 ou une vis de rappel isolante Optipress-Aquaplus 81042. |
|
|
Un revêtement ou une couche passive sur une surface métallique empêche le passage du courant de corrosion, p. ex. le bandage d’enroulement 83204 ou l’acier inoxydable comme matériau. |
|
|
La construction est constituée de métaux présentant un potentiel électrochimique à peu près identique. Ou alors, on renonce aux installations dites mixtes. |
|
|
La construction est réalisée de telle manière qu’un éventuel électrolyte ne puisse entrer en contact qu’avec un seul métal. |
Comment éviter la corrosion bimétallique (source: Informationsstelle Edelstahl Rostfrei, Düsseldorf, Merkblatt 829)
3.5 Corrosion surfacique
La corrosion surfacique a pour effet d’éroder un élément de construction sur toute sa surface à plus ou moins la même vitesse. Les parties d’une surface touchées par l’érosion par corrosion sont identifiables à une altération de la couleur. La corrosion surfacique peut entraîner une perte de poids importante de l’élément de construction concerné.
3.5.1 Aspect des dommages
La photo ci-dessous montre les dommages que la corrosion surfacique a causés à l’intérieur d’un tuyau en acier au carbone. Le tuyau provient d’une installation d’eau de boisson. L’oxygène dans l’eau de boisson a causé une corrosion par oxygène, avec pour conséquence l’érosion de la surface intérieure du tuyau.
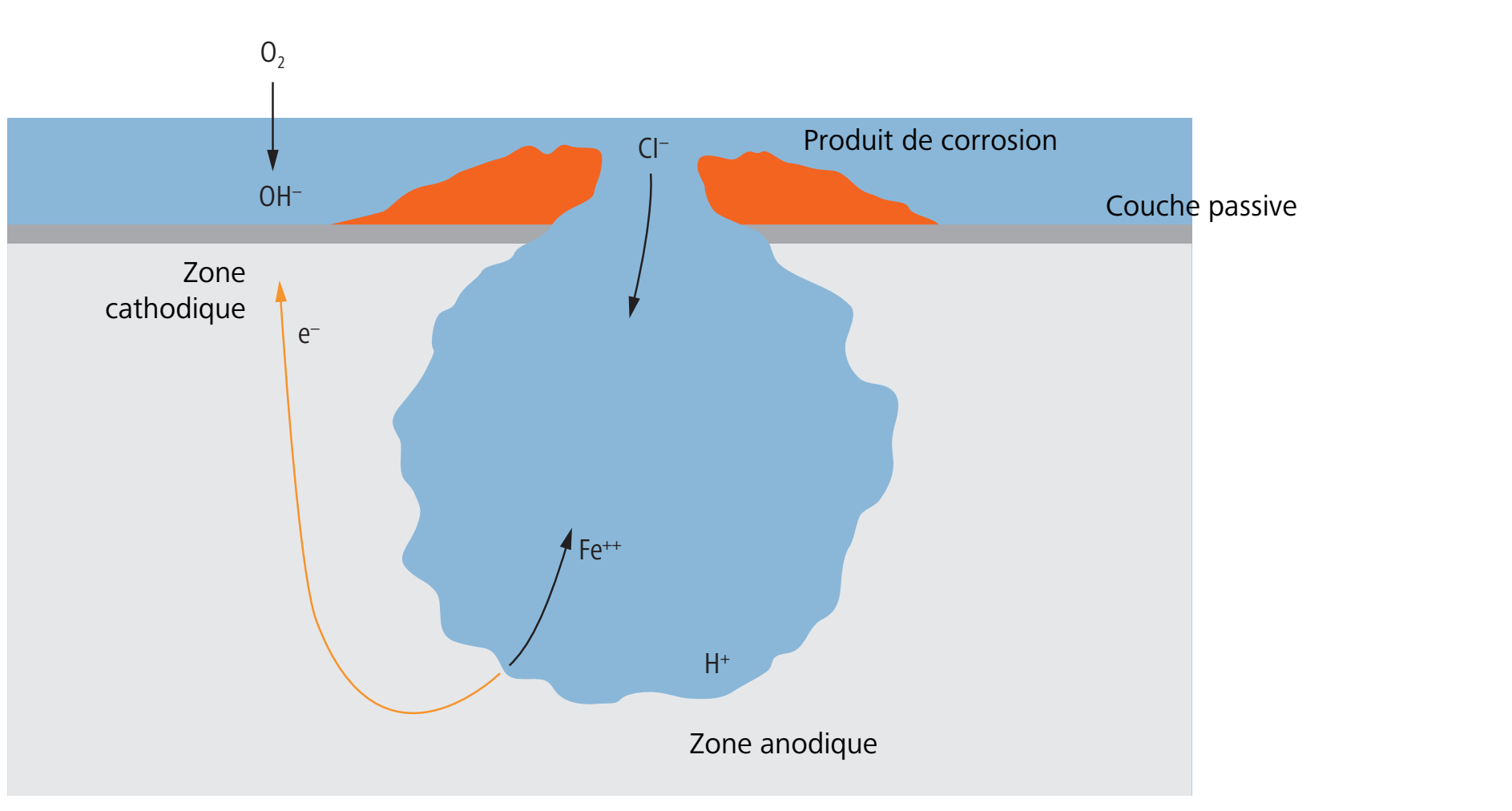
3.6 Corrosion par piqûres
La corrosion par piqûres est une corrosion locale et souvent très ponctuelle sur un élément de construction. Entre les endroits affectés par la corrosion par piqûres, il peut y avoir des surfaces qui ne sont pas touchées. La corrosion par piqûres peut progresser jusqu’à ce que l’élément de construction ne soit plus fonctionnel, p. ex. en raison d’un trou dans une conduite.
3.6.1 Corrosion par piqûres des aciers anticorrosion (indice PRE)
La corrosion par piqûres des aciers anticorrosion est causée surtout par des composés halogénés (composés de chlore, brome et iode). Les aciers anticorrosion dont l’alliage contient du molybdène ont une résistance accrue à la corrosion par piqûres.
Le potentiel de corrosion par piqûres mesure la résistance d’un acier anticorrosion contre la corrosion par piqûres. Ce potentiel est exprimé comme indice ou indice PRE (PRE: pitting resistance equivalent). La présence de molybdène dans l’alliage améliore nettement la résistance à la corrosion par piqûres. L’indice PRE est calculé à l’aide de la formule suivante:
Indice PRE = %Cr + 3.3 × %Mo
|
Symbole |
Unité |
Description |
|---|---|---|
|
Indice PRE |
— |
Potentiel de corrosion par piqûres |
|
%Cr |
Pourcentage de chrome dans l’alliage |
|
|
%Mo |
Pourcentage de molybdène dans l’alliage |
Plus l’indice PRE est élevé, plus la résistance contre la corrosion par piqûres est grande. Les types d’acier inoxydable utilisés dans les produits de
|
Type d’acier inoxydable |
Indice PRE |
Indice PRE (valeur normalisée) |
|---|---|---|
|
1.4521 |
24.1 |
23.0 |
|
1.4401/04 |
23.1 |
Indices PRE des types d’acier inoxydable de
3.6.2 Aspect des dommages
La photo ci-dessous montre les dommages causés par une corrosion par piqûres tellement avancée que la conduite a été percée.
3.6.3 Comment éviter la corrosion par piqûres
Pour l’isolation thermique de conduites, il faut utiliser des matériaux sans halogène.
L’étanchéité d’assemblages par filetage en acier anticorrosion doit être réalisée par du chanvre sans chlore ou d’autres produits d’étanchéité sans chlore. Les produits d’étanchéité pour filetage en matière synthétique comme le polytétrafluoroéthylène (PTFE) doivent être certifiés par l’organisme DVGW.
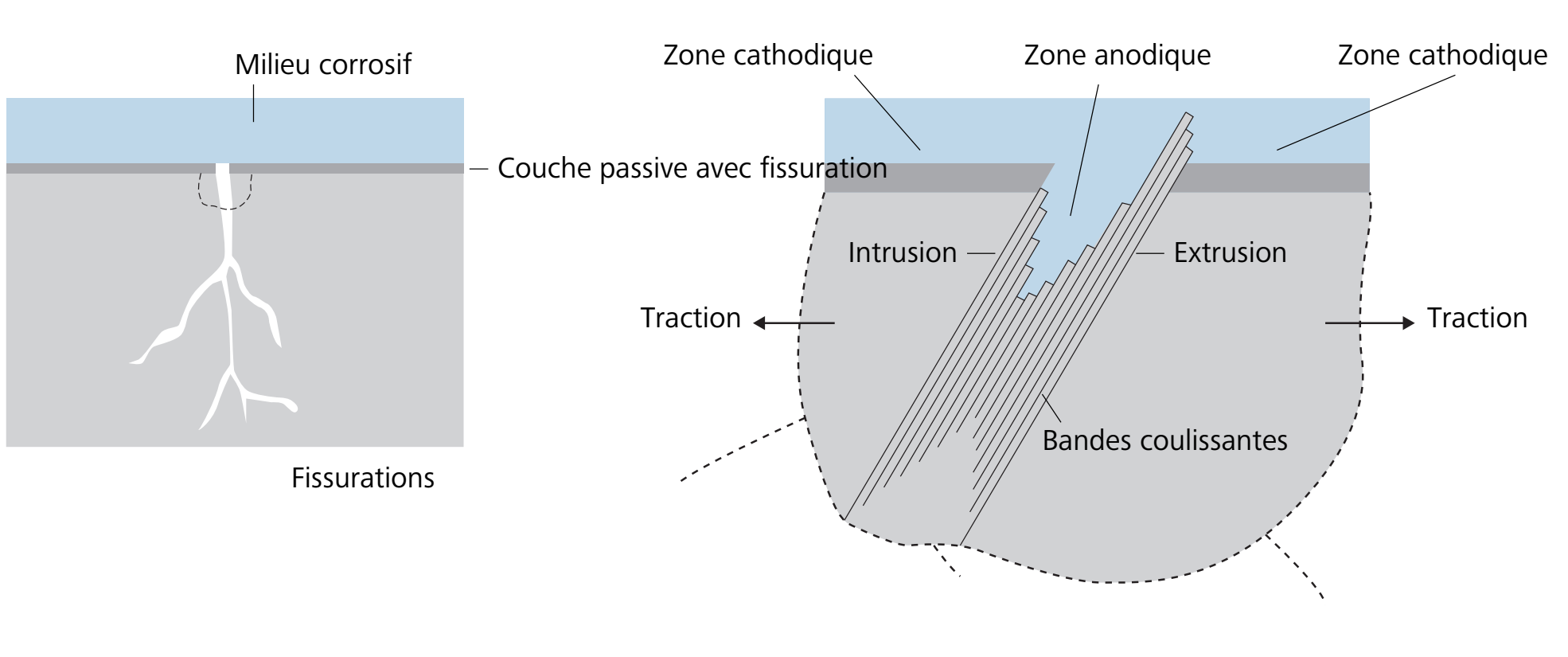
3.7 Corrosion fissurante sous tension
La corrosion fissurante sous tension désigne la fissuration d’une pièce en métal suite à de la corrosion et à son étirement par des tensions de traction.
La corrosion fissurante sous tension de métaux, en particulier d’aciers Cr-Ni austénitiques, est souvent causée par des solutions salines chlorées ou des composés chlorés humides. Les fissures sont souvent fortement ramifiées et courent perpendiculairement à la direction de la tension de traction à laquelle l’élément de construction est soumis. Ce type de corrosion est plutôt rare pour les aciers chromés ferritiques.
La corrosion fissurante sous tension peut apparaître sur des raccords en laiton qui sont entrés en contact avec de l’ammoniac ou de l’ammonium.
Les forces de traction susceptibles de déclencher une corrosion fissurante sous tension peuvent être présentes dans un élément de construction sous forme de tensions propres consécutives au processus de fabrication et d’usinage. Elles peuvent cependant aussi survenir lorsque le montage a été réalisé de manière conforme ou lors de sollicitations durant le fonctionnement de l’installation. A cet égard, une rallonge de robinet par exemple doit être considérée comme une utilisation critique, car l’expansion provoquée par le vissage se traduit par des tensions de traction. Ce qui est décisif à ce titre, c’est l’ampleur de la déformation pendant le montage ainsi que la dureté de l’élément de construction, qui donnent une indication indirecte de la plasticité. Pour une utilisation critique, le laiton doit être détendu thermiquement. A la sollicitation mécanique vient s’ajouter le fait que la corrosion fissurante sous tension est favorisée par certaines substances corrosives (p. ex. ammoniac, acide sulfurique). Le bronze résiste mieux que le laiton à la corrosion fissurante sous tension.
3.7.1 Aspect des dommages
La photo ci-dessous montre les dommages causés sur une douille coulissante par un début de corrosion fissurante sous tension.
La photo ci-dessous des dommages montre que la corrosion fissurante sous tension a abîmé un raccord fileté en laiton de 1¼ × 1 pouce.
3.8 Corrosion induite par un flux
Une corrosion induite par un flux désigne un processus résultant d’une interaction entre un fluide en circulation et une surface métallique. Elle revêt deux formes: la corrosion par érosion et la corrosion par cavitation. Comme les deux processus contrarient la formation de couches couvrantes protectrices, le matériau est exposé, ce qui favorise une corrosion sélective. Pour le cuivre et les alliages de cuivre, ce phénomène est particulièrement critique car leur résistance dépend de l’absence de défauts de la structure des couches couvrantes protectrices.
3.8.1 Corrosion par érosion
La norme SN EN 12502-2:2004 décrit la corrosion par érosion comme étant un décapage local de matière, souvent associé à une corrosion chimique.
3.8.1.1 Erosion
Le processus physique de l’érosion dans les systèmes de conduites se présente lorsque l’écoulement de l’eau a une action mécanique sur la surface des conduites et les décape progressivement. Causes fréquentes:
-
Vitesses d’écoulement élevées: L’écoulement rapide de l’eau peut avoir une action directe sur la paroi des tuyaux et les décaper.
-
Particules abrasives: Les particules en suspension dans l’eau telles que le sable ou tout autre matériau solide peuvent endommager la paroi intérieure des tuyaux par frottement.
-
Ecoulement turbulent: Tout changement subit de la direction d’écoulement ou tout rétrécissement des conduites peut avoir pour effet d’accélérer le flux et de décaper de la matière.
L’érosion conduit à une perte progressive de matière et donc à une réduction de l’épaisseur de la paroi des tuyaux, ce qui peut en altérer leur résistance structurelle.
3.8.1.2 Conséquences
-
La couche couvrante est endommagée ou sa formation est perturbée, p. ex. la couche protectrice d’oxyde et de carbonate sur les surfaces en cuivre.
-
La surface métallique débarrassée de sa couche couvrante est exposée à une corrosion chimique plus importante étant donné que l’échange d’ions n’est plus entravé.
-
La corrosion chimique se caractérise par des mini-trous caractéristiques en forme de fer à cheval.
-
Dans les systèmes d’approvisionnement en eau chaude, la corrosion par l’érosion se produit souvent aux endroits où l’écoulement change brusquement de direction, p. ex. aux arêtes.
3.8.1.3 Pour éviter les phénomènes indésirables
La norme EN 12502-2 contient des recommandations sur les vitesses d’écoulement maximales et sur la conception des conduites. Il s’agit de valeurs indicatives utiles à la planification et à l’exploitation de conduites véhiculant de l’eau.
Valeurs limites pour les vitesses d’écoulement:
-
Conduites en cuivre:
-
Temps de soutirage courts: max. 3 m/s
-
Temps de soutirage longs (>15 minutes): max. 2 m/s
-
Dans les systèmes de circulation pour l’approvisionnement en eau chaude: max. 0.5 m/s
-
-
Pour les conduites en alliage de cuivre, les valeurs limites sont les mêmes que pour les conduites en cuivre. Des vitesses d’écoulement supérieures sont cependant possibles lorsque la résistance à la corrosion est plus élevée.
-
Conduites en bronze: Dans les systèmes de circulation pour l’approvisionnement en eau chaude: max. 1 m/s, en fonction de la composition de l’eau et de la conception des conduites
Pour éviter les turbulences dans les conduites:
-
Pas de changements brusques de section et de direction des conduites.
-
Eléments stabilisant le flux, p. ex. tronçon de conduite rectiligne après une pompe de circulation.
-
Minimiser le nombre de tuyaux cintrés et de robinets dans le réseau de conduites.
Choix des matériaux:
-
Lorsqu’il n’est pas possible de se conformer aux vitesses d’écoulement recommandées par la norme EN 12502-2, il convient d’utiliser plutôt de l’acier inoxydable que du cuivre et des alliages de cuivre. L’acier inoxydable résiste mieux à la corrosion et est plus adapté à des conditions d’écoulement critiques.
-
Si la norme EN 12502-2 peut être respectée, il faut choisir des alliages de cuivre qui ont une plus forte résistance à l’érosion. De manière générale, éviter le laiton et utiliser le bronze car il résiste mieux à la corrosion par érosion.
3.8.1.4 Aspect des dommages
La photo ci-dessous montre les dommages causés par la corrosion par érosion sur un robinet oblique dans une conduite de circulation. Le blocage mécanique de l’élément de retenue (pas sur la photo) a permis d’accroître les performances de la pompe de circulation afin de maintenir le débit volumique de la conduite de circulation. Conséquences: vitesses d’écoulement élevées au niveau du clapet porte-joint et flux turbulent, ce qui provoque une corrosion par érosion.
3.8.2 Corrosion par cavitation
La corrosion par cavitation est un phénomène de creusement qui abîme la surface d’un métal par une action mécanique, favorisant ainsi une corrosion chimique.
3.8.2.1 Cavitation
Le processus physique de la cavitation est le fait de différences localisées dans la pression d’un liquide, ce qui conduit à la formation de bulles de gaz qui finissent par éclater. La cavitation dans les conduites peut avoir plusieurs origines:
-
Fluctuations dans la pression: Dans les tronçons aux vitesses d’écoulement élevées ou dans les sections étroites, la pression peut localement connaître une telle chute que l’eau s’évapore en formant des bulles de gaz.
-
Implosion des bulles: Les bulles implosent lorsqu’elles traversent des tronçons à pression élevée. Les coups de bélier qu’elles provoquent sont susceptibles d’endommager la paroi des conduites.
-
Effet récurrent: Lorsque l’éclatement de bulles est récurrent, le décapage systématique de la matière peut prendre une telle ampleur que l’on parle d’une érosion par cavitation.
La cavitation cause des dommages locaux caractérisés par des mini-trous ou piqûres dans la paroi des conduites. Ces dommages peuvent s’étendre et, par la suite, altérer la fonction de la conduite.
3.8.2.2 Conséquences
-
La corrosion par cavitation est un phénomène typique dans les pompes, robinets ou sections étroites de conduites qui présentent de grosses différences de pression.
-
Dommages causés aux matériaux avec bosses évoquant la variole.
-
En particulier pour les alliages de cuivre:
-
la couche couvrante, p. ex le carbonate de cuivre basique, est endommagée par la cavitation.
-
Le métal exposé est soumis à une corrosion sélective, en particulier dans les eaux acides et chargées en sulfates.
-
3.8.2.3 Pour éviter les phénomènes indésirables
Les conditions d’écoulement et la nature de l’eau sont des facteurs critiques pouvant déclencher la corrosion par cavitation:
-
Eviter les vitesses d’écoulement trop élevées et les changements de pression brusques, p. ex. sur les pompes et éléments d’étranglement.
-
Eviter les eaux saturées en gaz. Les eaux saturées en gaz favorisent la formation de bulles de gaz, p. ex. lors du dégazage incontrôlé des conduites.
-
A prendre en compte spécifiquement pour les conduites en cuivre et en alliages de cuivre:
-
Réduire la formation de bulles de gaz par des dispositifs de dégazage.
-
Eviter les chutes de pression par le dimensionnement suffisant des conduites et des pompes.
-
3.8.2.4 Aspect des dommages
La photo suivante montre la corrosion par cavitation provoquée dans des conditions de laboratoire sur une plaque d’essai en bronze sans plomb. A cet effet, la plaque d’essai et une sonotrode à ultrasons ont été plongées dans un récipient rempli d’eau. La plaque a ensuite été exposée à l’action de la sonotrode à ultrasons pendant un certain temps. Les ultrasons ont provoqué une cavitation sous l’effet d’un décapage visible de matière à la surface de la plaque.
La photo suivante montre une forme mixte de corrosion par érosion et cavitation sur un réducteur de pression.
3.9 Corrosion sélective
La corrosion sélective est la corrosion d’un alliage où ses composants forment un élément de corrosion en raison des différences de potentiels électrochimiques, l’électrolyte correspondant dans de nombreux à de l’eau. Le composant d’alliage le moins noble se corrode le long de la microstructure du matériau. Quant au composant d’alliage le plus noble, il subsiste dans le matériau à l’état poreux. Pour la corrosion sélective, on peut citer comme exemple la dézincification du laiton.
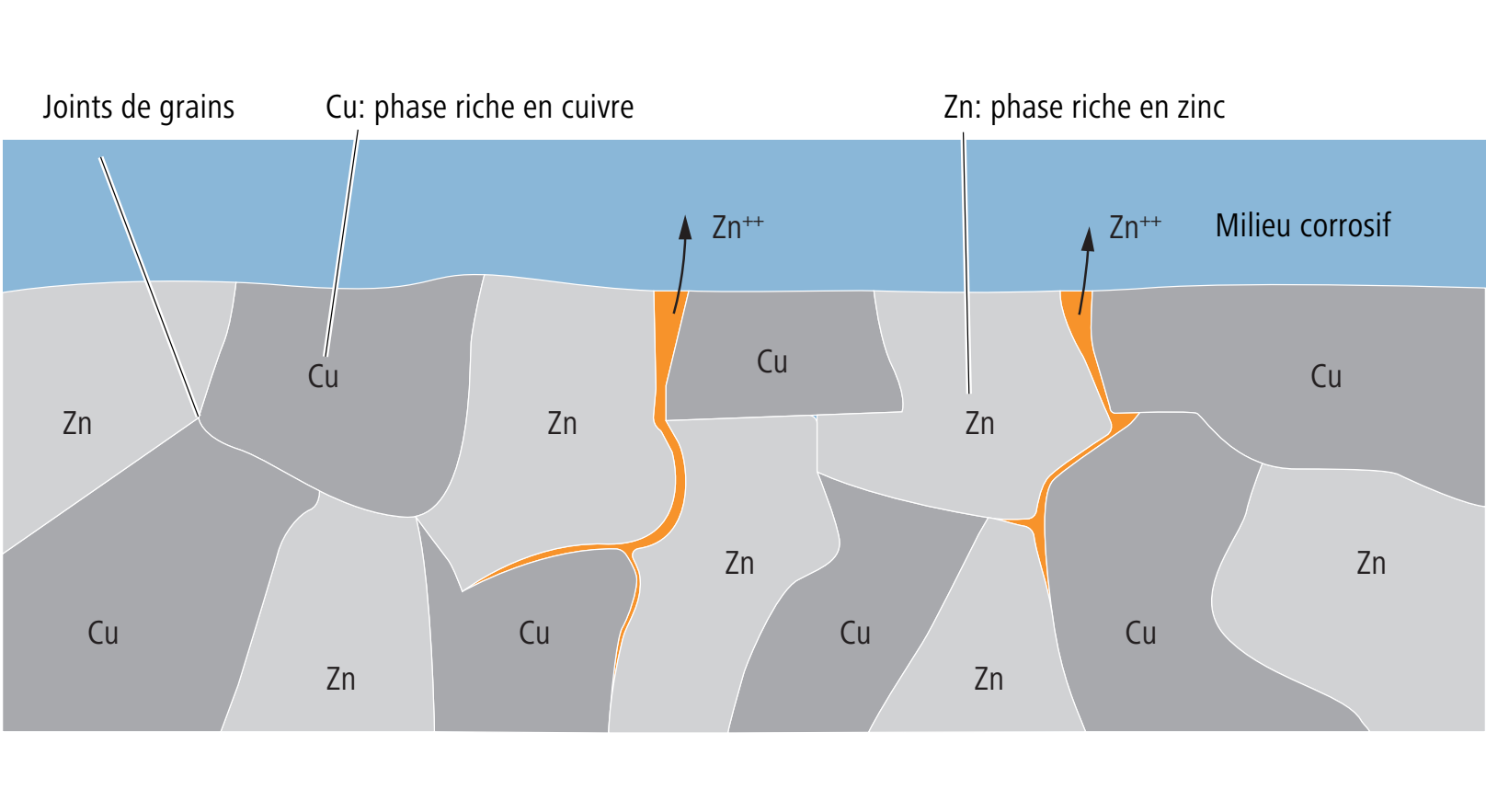
3.9.1 Dézincification
Pour la corrosion sélective, on peut citer comme exemple la dézincification d’éléments de conduites en laiton. Lors de la dézincification, la corrosion fait disparaître le zinc dans le laiton, après quoi il ne subsiste que du cuivre poreux. La présence de croûtes de sel sur l’extérieur de robinetteries en laiton peut être un signe de dézincification, un phénomène qui peut se produire dans les conduites d’eau chaude en particulier.
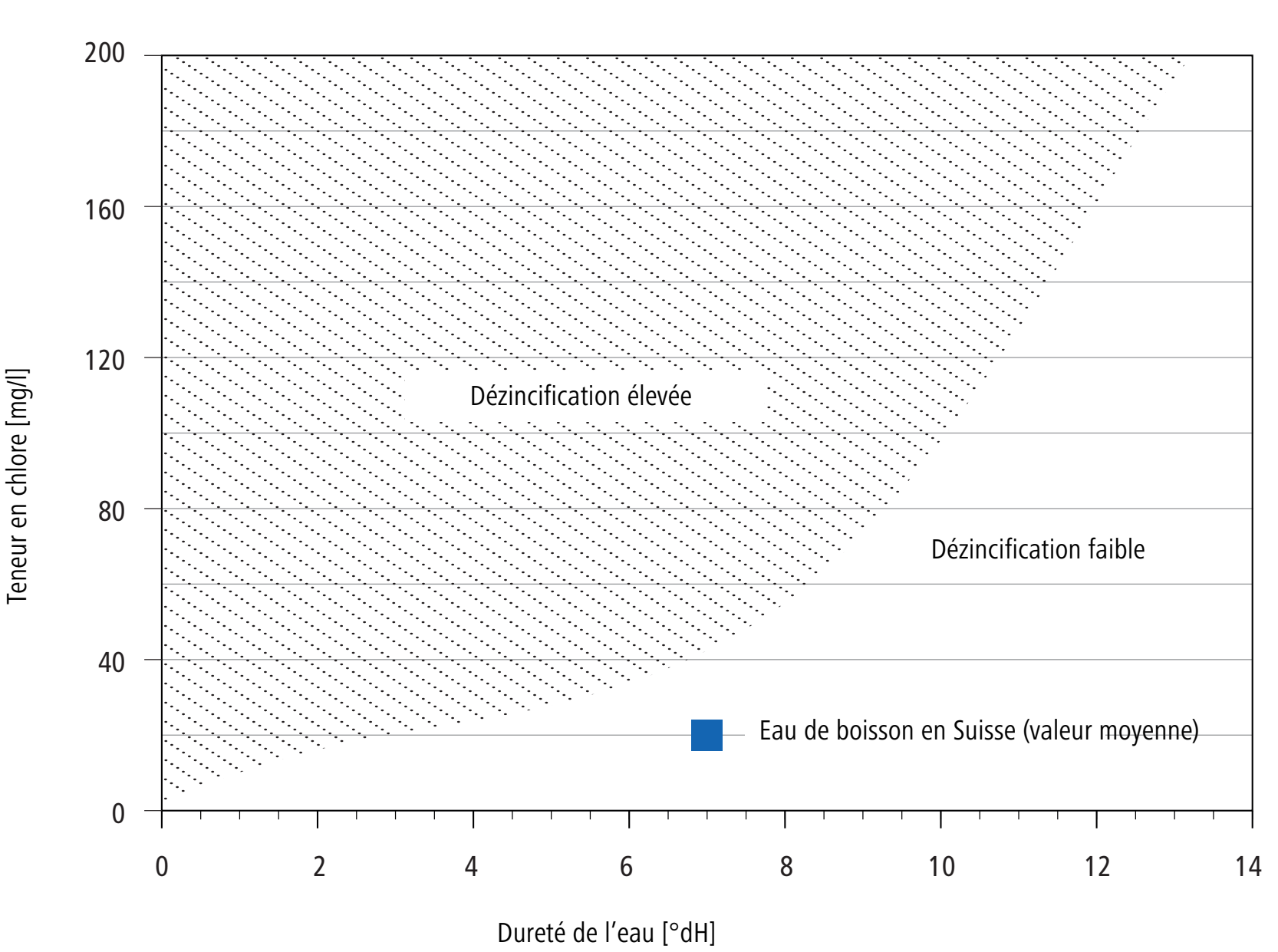
3.9.2 Diagramme de Turner
La composition de l’eau a une incidence sur la dézincification du laiton. Une dureté élevée de l’eau et une faible teneur en chlore s’opposent à une dézincification. Le rapport entre dézincification, dureté de l’eau et teneur en chlore apparaît dans le diagramme de Turner.
3.9.3 Aspect des dommages
La photo ci-dessous des dommages montre la dézincification sur le filetage d’une tête de robinet. La structure de l’élément de construction a été tellement affaiblie par la perte progressive de zinc que son filetage ne résiste plus au vissage.
3.10 Corrosion intercristalline
On désigne par corrosion intercristalline la corrosion dans ou à côté des joints de grains dans un alliage métallique.
La corrosion intercristalline est favorisée par une microstructure à gros grains, une part importante des éléments d’alliage arsenic et phosphore dans le matériau, de même que par des températures élevées. De l’ammoniac dans l’eau et des éléments d’aération peuvent également être à l’origine de la corrosion intercristalline.
Les alliages en laiton sont exposés à la corrosion intercristalline lorsqu’il y a des précipitations aux joints de grains. La dézincification du laiton peut être due à une corrosion par piqûres ou à une corrosion intercristalline.
3.10.1 Aspect des dommages
La photo ci-dessous montre les dommages que la corrosion intercristalline a causés sur un élément de construction en laiton.
Lorsqu’un élément de construction subit des tensions de traction mécaniques auxquelles s’ajoute une corrosion intercristalline, cela peut causer des fissures de contrainte, comme le montre la photo ci-dessous:
3.11 Corrosion par courant vagabond
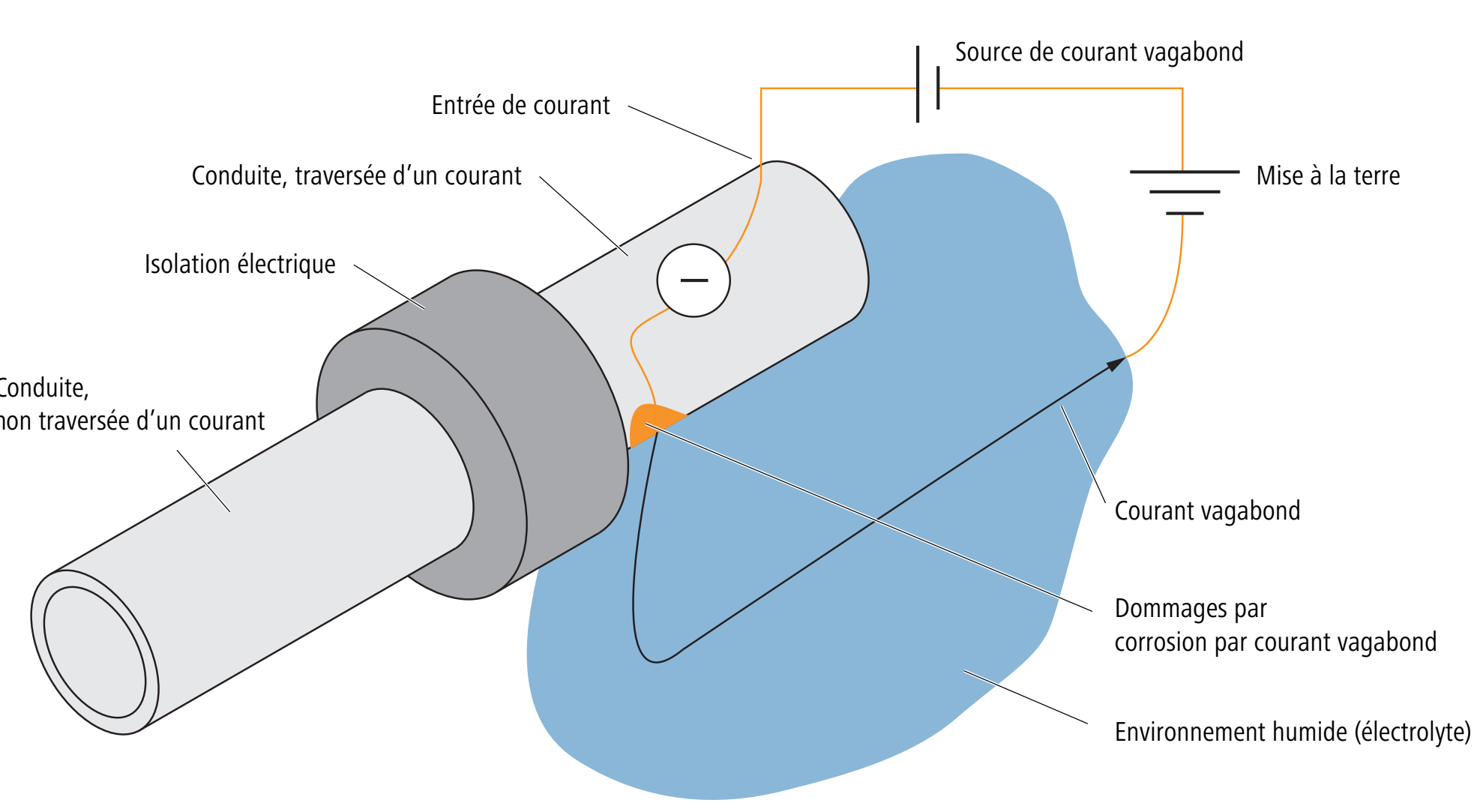
La corrosion par courant vagabond est une corrosion électrochimique due à des courants vagabonds. Les courants vagabonds (dits aussi courants vagabonds) peuvent se manifester lorsque des courants électriques sont dérivés dans le sol par une mise à la terre et s’ils sont détournés par des isolations ou des résistances. Il peut s’agir de courant continu ou alternatif, seul le courant continu pouvant entrer en ligne de compte pour la corrosion.
Lorsqu’un courant continu traverse une pièce métallique située dans un environnement humide, il peut arriver que soit déclenchée une réaction partielle anodique du métal en présence d’oxygène. Il s’ensuit une corrosion de la pièce métallique.
L’isolation électrique dans le schéma sert à montrer la déviation du courant vagabond de la conduite vers un environnement à faible impédance, en sachant qu’il peut y avoir de la corrosion aux sorties.
3.11.1 Comment éviter la corrosion par courant vagabond
La corrosion par courant vagabond sur une installation sanitaire peut être due aux raccordements électriques du bâtiment. Selon le système de réseau et les consommateurs, les courants vagabonds peuvent se manifester dans des conduites, installations de chauffage et de ventilation, dispositifs de protection contre la foudre et éléments de colombage mécaniques. Si en plus de l’humidité entre en jeu, il peut y avoir de la corrosion.
Dans les systèmes de TN, les conducteurs actifs du réseau électrique sont reliés via le point étoile du transformateur avec le potentiel de terre, les consommateurs électriques étant, quant à eux, raccordés de deux manières différentes à ce point:
-
Dans le réseau TN-C (terre neutre combiné), cela se fait via le conducteur PEN qui réunit les fonctions du conducteur de protection (PE) et du conducteur neutre (N).
-
Dans le réseau TN-S (terre neutre séparé), les conducteurs neutre et de protection sont posés séparément.
Lorsque les deux systèmes de réseau sont réunis, on parle de réseau TN-C-S.
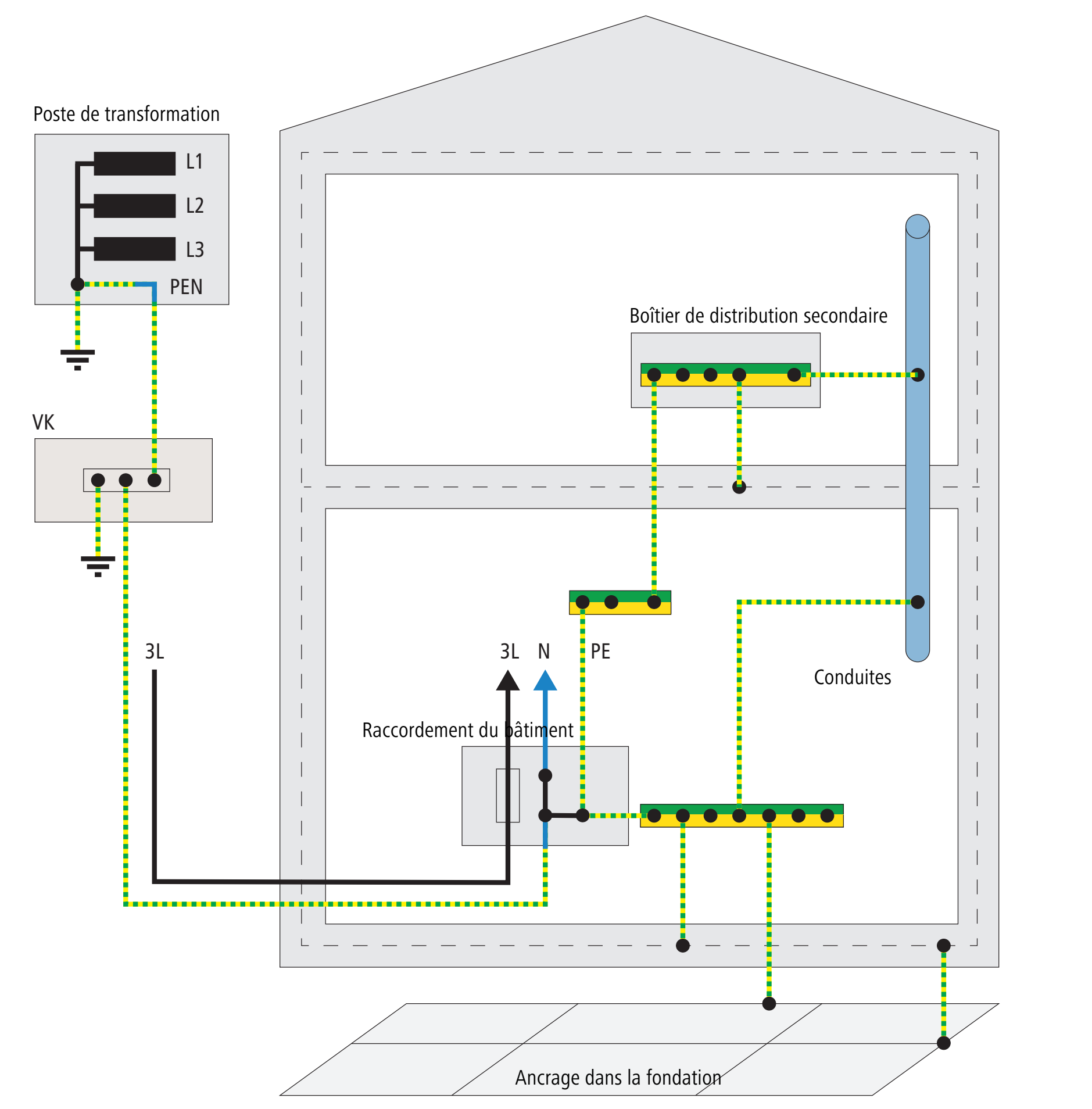
3.11.1.1 Système de réseau TN-C
Le système TN-C possède un conducteur PEN commun pour les connexions entre le coffret de raccordement du bâtiment et les boîtiers de distribution secondaire. Souvent, ce n’est que dans le circuit vers le consommateur qu’il y a un conducteur de protection séparé (PE).
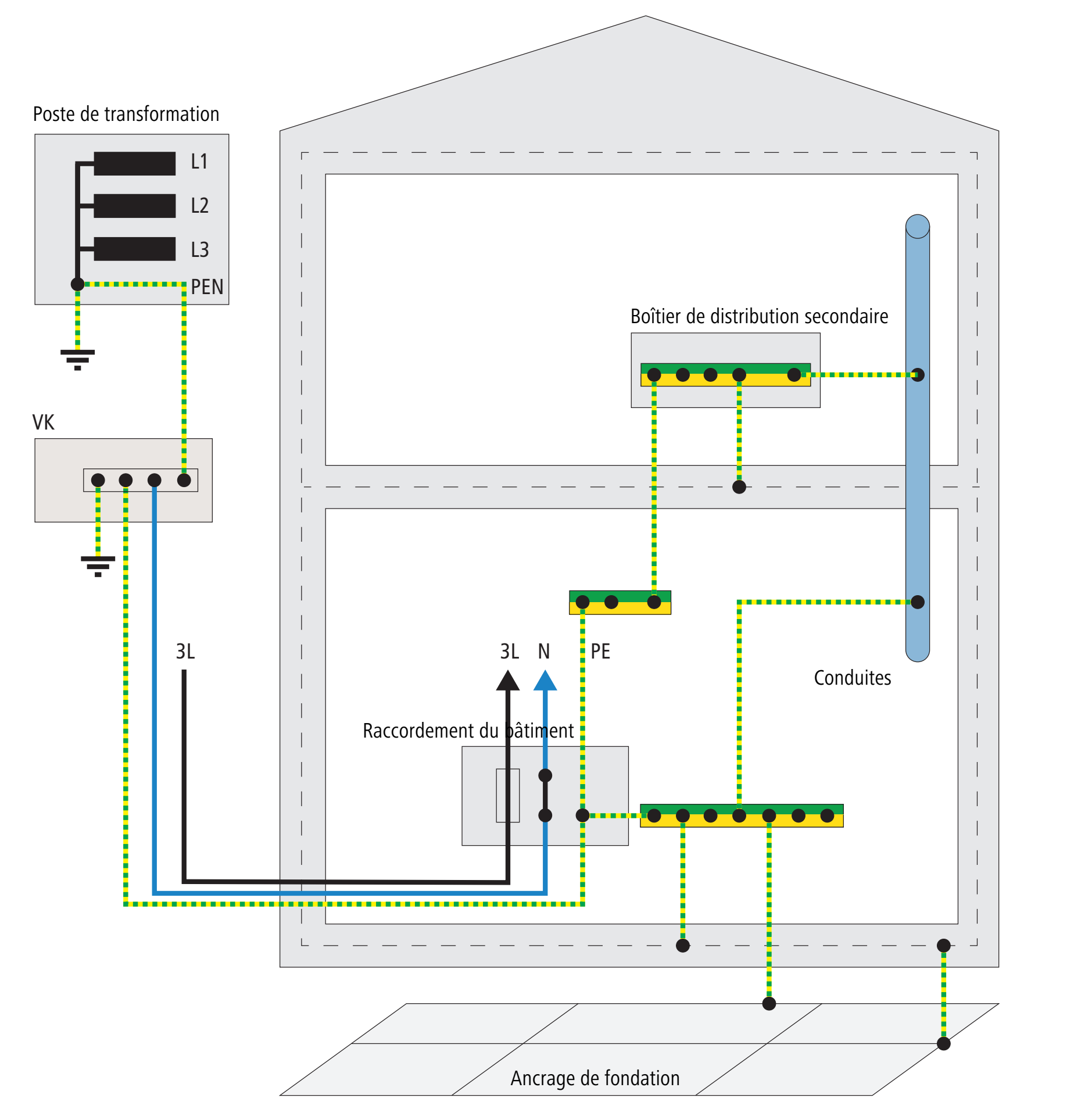
3.11.1.2 Système de réseau TN-S
Le système de réseau TN-S présente, au niveau du raccordement électrique du bâtiment, un embranchement du conducteur PEN en conducteur de protection et conducteur neutre.
3.11.1.3 Mise à la terre d’installations électriques
Une mise à la terre d’installations électriques dans un bâtiment correspond à un dispositif de protection électrique qui, lors d’un dysfonctionnement, empêche que les parties non conductrices d’électricité soient mises sous tension.
La mise à la terre par le réseau de distribution d’eau de boisson n’est pas recommandée pour les raisons suivantes:
-
Les courants vagabonds issus d’installations électriques risquent de traverser le réseau de distribution d’eau de boisson, avec pour conséquence une corrosion par courant vagabond.
-
La mise à la terre risque d’être coupée lors du remplacement ou de la réparation de conduites (métalliques).
Dans le cas d’une mise à la terre par les conduites de raccordement d’eau du bâtiment, la source de courant vagabond peut être située très loin du bâtiment. Cela peut rendre très compliquée la localisation de sources de courant vagabond et le blocage de celles-ci. En outre, il faut tenir compte du fait que le nombre de sources de courant vagabond ne fait que croître en raison de la multiplication de l’utilisation d’appareils électriques. Il faut savoir aussi que les consommateurs non linéaires prennent une place toujours plus importante comme source de perturbation.
Alternativement, on peut envisager les mises à la terre suivantes:
-
Electrode de terre de fondation
-
Rubans de terre
-
Piquets de terre
-
Autres pièces de construction fichées dans la terre
|
1 |
Raccordement d’eau du bâtiment |
|
2 |
Electrode de terre de fondation (fait partie de l’armature du mur) |
|
3 |
Conducteur de protection d’installations électriques |
|
4 |
Rubans de terre |
|
5 |
Câble ou pontage de fil |
La mise à la terre d’installations électriques doit être réalisée et contrôlée par des électriciens.
3.12 Biocorrosion (MIC)
La biocorrosion, dite aussi corrosion microbienne (MIC pour microbial influenced corrosion), est un processus microbien qui accélère la corrosion des métaux. Les bactéries sidérophiles et bactéries réductrices de sulfates y jouent un rôle important.
-
Les bactéries sidérophiles (IRB pour iron relevant bacteria) sont des microorganismes aérobiques qui se servent des oxydes de fer comme source d’énergie. Les bactéries sidérophiles oxydent le fer bivalent (Fe²⁺) en fer trivalent (Fe³⁺), ce qui conduit à la formation de dépôts d’oxydes et d’hydroxydes de fer. Ces dépôts sont susceptibles de couvrir les surfaces en métal et d’en accélérer la corrosion.
-
Les bactéries sulfato-réductrices (SRB pour sulfat reducing bacteria) sont des microorganismes anaérobiques qui réduisent les sulfates (SO₄²⁻) en sulfites (S²⁻). Les sulfites ainsi formés peuvent réagir avec du fer et former un sulfite de fer, ce qui entraîne la formation d’une couche noire et boueuse sur la surface métallique. Cette couche peut à son tour favoriser la corrosion.
Contrairement à d’autres types de corrosion, la biocorrosion ne dépend pas de la concentration d’oxygène. Les bactéries sulfato-réductrices se multiplient dans des environnements pauvres en oxygène. Les bactéries sidérophiles sont actives en présence d’oxygène. C’est pourquoi la biocorrosion peut se produire aussi bien dans des environnements riches que pauvres en oxygène.
3.12.1 Aspects rencontrés
La biocorrosion peut revêtir divers aspects selon les microorganismes qui interviennent dans sa formation:
-
Les bactéries sidérophiles forment des dépôts de couleur rouille ou brune à la surface du métal.
-
Les bactéries sulfato-réductrices forment, quant à elles, des dépôts noirs et boueux pouvant dégager une odeur d’œufs pourris (due à la formation d’hydrogène sulfuré).
3.12.2 Biocorrosion dans les installations sprinklers
La biocorrosion peut créer des fuites dans les installations sprinklers et en altérer le fonctionnement. La stagnation de l’eau dans les installations sprinklers favorise la prolifération des microorganismes,surtout sur des installations rarement activées. Les conduites en fer galvanisé sont particulièrement sujettes à la biocorrosion, car la couche de zinc est attaquée par l’activité des bactéries sulfato-réductrices et sidérophiles. L’utilisation d’acier inoxydable dans les installations sprinklers peut réduire considérablement la biocorrosion.
3.12.3 Aspect des dommages
La photo suivante montre les dommages causés par la biocorrosion due à des bactéries sidérophiles (IRB) sur la paroi interne d’un tuyau en acier C non galvanisé. Après le démontage du tuyau, la partie à gauche de la ligne bleue a été nettoyée, la partie à droite ayant été laissée en l’état.
La photo suivante montre les dommages causés par la biocorrosion due à des bactéries sulfato-réductrices (SRB) sur un élément d’armoire de commande en cuivre.