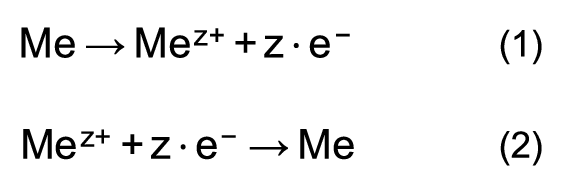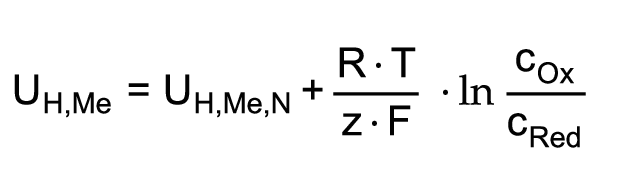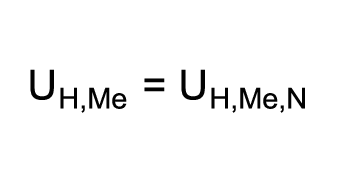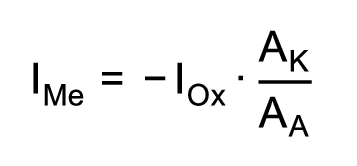Themenwelt - Korrosion
2.1 Potentialbildung
Das Potential ist eine Eigenschaft von Metallen wie die Härte oder die elektrische Leitfähigkeit und ist immer in Verbindung mit einer wässrigen Lösung zu verstehen, in der sich das Metall befindet.
Wenn ein Metall in eine wässrige Lösung eingetaucht wird, herrschen zwischen dem Metall und der wässrigen Lösung thermodynamische Ungleichgewichtszustände, die u. a. auf unterschiedliche Stoffkonzentrationen in den beiden Phasen zurückzuführen sind. Diese Ungleichgewichtszustände haben Wechselwirkungen zur Folge, die durch Bewegungen von Ionen und Elektronen gekennzeichnet sind. Dabei gehen Ionen vom Metall in die wässrige Lösung und von der wässrigen Lösung zum Metall über. Diese Übergangsbewegungen sind elektrochemische Reaktionen und finden solange statt, bis der thermodynamische Gleichgewichtszustand erreicht ist. Da Ionen elektrische Ladungsträger sind, kommt es dabei zu Potentialänderungen, dementsprechend bestimmen die Ionen, d. h. deren Anzahl und elektrische Ladung, das Potential eines Metalls.
Die beiden Reaktionen lassen sich mit den folgenden Reaktionsformeln darstellen:
|
Formelzeichen |
Einheit |
Beschreibung |
|---|---|---|
|
Me |
— |
Metall, im atomaren Zustand |
|
Mez+ |
Metall-Ion, z-wertig (positive Ladungseinheit) |
|
|
z |
Anzahl Elektronen |
|
|
e− |
Elektron (negative Ladungseinheit) |
Die Reaktionsformel (1) beschreibt die Metallauflösung. Die Ionen bewegen sich vom Metall in die wässrige Lösung. Dieser Vorgang wird auch als Lösungsdruck bezeichnet. Weitere Bezeichnungen sind Anodenvorgang oder anodische Reaktion.
Die Reaktionsformel (2) beschreibt die Metallabscheidung. Die Ionen bewegen sich aus der wässrigen Lösung zum Metall. Dieser Vorgang wird auch als osmotischer Druck bezeichnet. Weitere Bezeichnungen sind Kathodenvorgang oder kathodische Reaktion.
Die beiden Reaktionen laufen beim Eintauchen eines Metalls gleichzeitig ab, jedoch meistens mit unterschiedlichen Geschwindigkeiten. Wenn Reaktion (1) schneller abläuft als Reaktion (2), dann wird das Metall durch die Ansammlung von Elektronen zu Beginn der Reaktionen negativ aufgeladen. So reagierende Metalle werden als unedel bezeichnet. Im umgekehrten Fall wird das Metall durch die grössere Abscheidungsgeschwindigkeit positiv aufgeladen. Solche Metalle werden als edel bezeichnet.
An den Schichten der Phasengrenze Metall/Lösung entsteht also eine Potentialdifferenz, die mit der Potentialdifferenz zwischen den Platten eines Kondensators vergleichbar ist. Diese elektrische Spannung wird als Galvani-Spannung bezeichnet und kann nicht gemessen werden.
2.2 Potentialmessung
Das Potential eines Metalls kann nur relativ zum Potential eines zweiten Metalls gemessen werden, d. h. man misst die Differenz der beiden Galvani-Spannungen. Diese Spannungsdifferenz wird als Elektrodenpotential* bezeichnet.
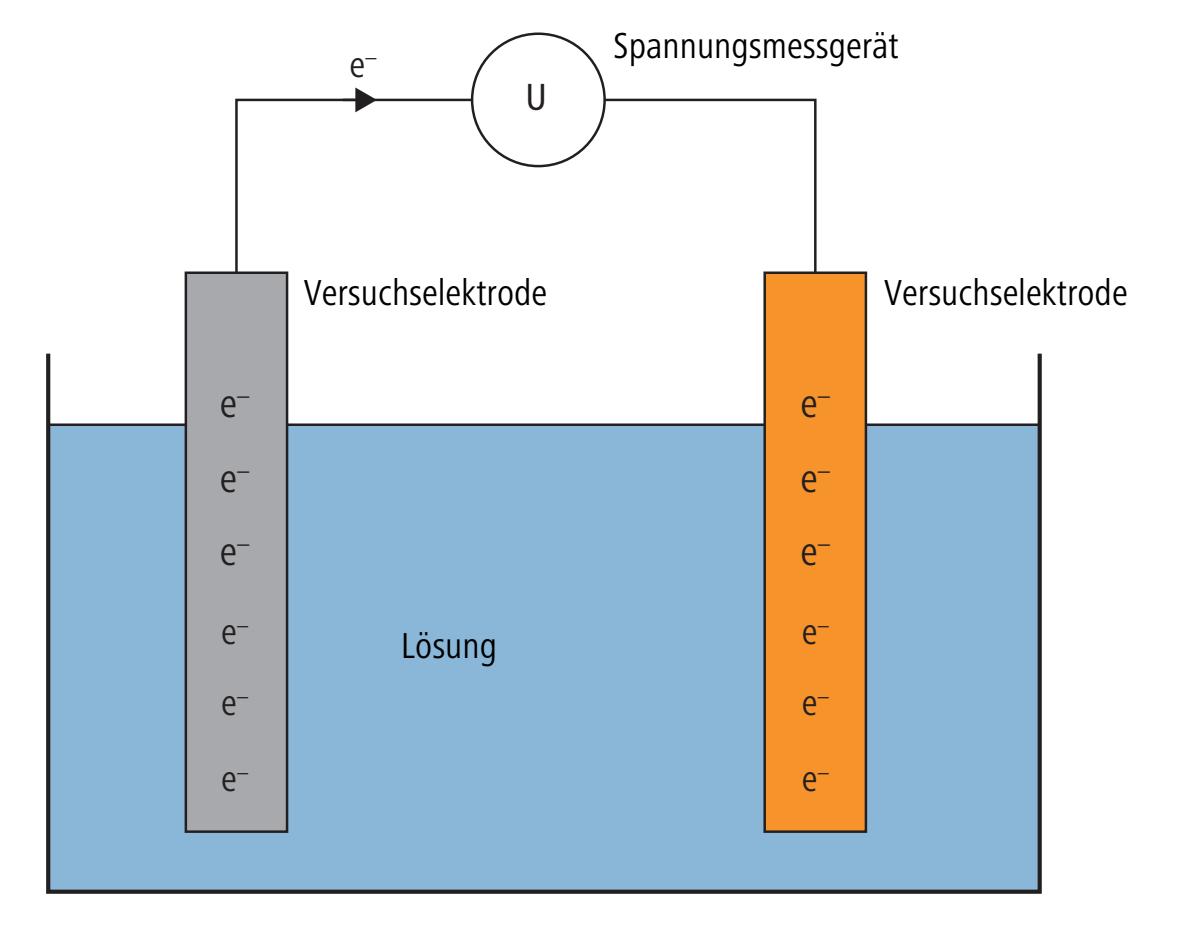
Das folgende Bild zeigt die Messvorrichtung zur Messung des Elektrodenpotentials zwischen der Versuchselektrode und einer Bezugselektrode. Bei unterschiedlichen Galvani-Spannungen der Versuchselektrode und der Bezugselektrode zeigt das Spannungsmessgerät eine Spannung an.
Um die Elektrodenpotentiale von verschiedenen Metallen für Vergleichszwecke zu messen, müsste die Galvani-Spannung von jedem Metall bekannt sein. Die Galvani-Spannung kann aber weder gemessen noch berechnet werden. Daher wurde das Elektrodenpotential von Wasserstoff mit dem frei gewählten Wert von 0 Volt als Standardpotential (oder Normalpotential) definiert, wobei die Lösungstemperatur 25 °C und die Lösungskonzentration 1 mol/Liter beträgt. Anhand des so definierten Standardpotentials ist es möglich, verschiedene Metalle miteinander zu vergleichen.
Aus praktischen Gründen wird als Bezugselektrode nicht Wasserstoff, sondern eine andere Elektrode gewählt, z. B. die Kalomel-Elektrode. Die Kalomel-Elektrode weist ein Elektrodenpotential von 0.25 Volt gegenüber dem Standardpotential von Wasserstoff auf.
* Die Bezeichnung Elektrodenpotential ist genau genommen falsch, da es sich um eine Potentialdifferenz, also um eine Spannung handelt.
2.3 Nernst-Gleichung
Um das Elektrodenpotential von verschiedenen Metallen miteinander zu vergleichen, ist neben der Bezugselektrode auch die wässrige Lösung (Elektrolyt) zu berücksichtigen. Denn schon einfache Experimente zeigen, dass ein Metall in Lösungen von gleicher chemischer Zusammensetzung, aber verschiedenen Stoffkonzentrationen unterschiedlich reagiert.
Der Zusammenhang zwischen dem Elektrodenpotential eines Metalls und der Konzentration der potentialbildenden Ionen wird durch die Nernst-Gleichung ausgedrückt:
|
Formelzeichen |
Einheit |
Beschreibung |
|---|---|---|
|
UH,Me |
V |
Elektrodenpotential des Metalls Me |
|
UH,Me,N |
V |
Normalpotential des Metalls Me gegenüber der Normalwasserstoffelektrode |
|
R |
J/(mol⋅K) |
Gaskonstante 8.31447 |
|
z |
— |
Anzahl Elektronen |
|
F |
J/(V⋅mol) |
Faraday-Konstante 96485 |
|
cOx |
mol/l |
Stoffkonzentration des Oxidationsmittels |
|
cRed |
mol/l |
Stoffkonzentration des Reduktionsmittels |
Die Gleichung zeigt, dass das Elektrodenpotential ansteigt, wenn
-
die Stoffkonzentration des Oxidationsmittels in der Lösung erhöht wird
-
die Temperatur der Lösung erhöht wird
Als Beispiel für eine Lösung kann die Salzsäure (HCl) herangezogen werden. Eine stark konzentrierte Salzsäure enthält eine höhere Stoffkonzentration des Oxidationsmittels H2. Das Elektrodenpotential des in der Salzsäure befindlichen Metalls steigt und damit auch dessen Reaktion. Dies ist auch der Fall, wenn die Temperatur der Salzsäure erhöht wird.
Die folgende Gleichung stellt die vereinfachte Form der Nernst-Gleichung dar. Sie gilt nur bei einer Lösungstemperatur von 25 °C und für verdünnte Lösungen, die bei Korrosion oft auftreten:
|
Formelzeichen |
Einheit |
Beschreibung |
|---|---|---|
|
UH,Me |
V |
Elektrodenpotential des Metalls Me |
|
UH,Me,N |
V |
Normalpotential des Metalls Me gegenüber der Normalwasserstoffelektrode |
|
z |
— |
Anzahl Elektronen |
|
cMe |
mol/l |
Stoffkonzentration der Metallionen (Dekadischer Logarithmus) |
Wenn in der vereinfachten Nernst-Gleichung die Stoffkonzentration cMe von 1 mol/l eingesetzt wird, dann ist der logarithmische Teil der Gleichung gleich Null (log1 = 0). Man erhält die folgende Gleichung:
Die Gleichung drückt aus, dass das Elektrodenpotential eines Metalls gleich seinem Normalpotential ist, wenn das Metall in eine Lösung von 1 mol/l Stoffkonzentration seiner Metallionen getaucht ist. Die Gleichung definiert das Normalpotential und bildet somit eine Grundlage zur Erstellung von elektrochemischen Spannungsreihen.
2.4 Elektrochemische Spannungsreihe
Elektrochemische Spannungsreihen dienen zum Vergleich der Potentiale von Metallen. In vielen elektrochemischen Reihen wird als Vergleichsgrösse das Normalpotential und als Bezugselektrode die Normalwasserstoffelektrode verwendet. Es können durch Messungen aber auch andere elektrochemische Spannungsreihen erstellt werden.
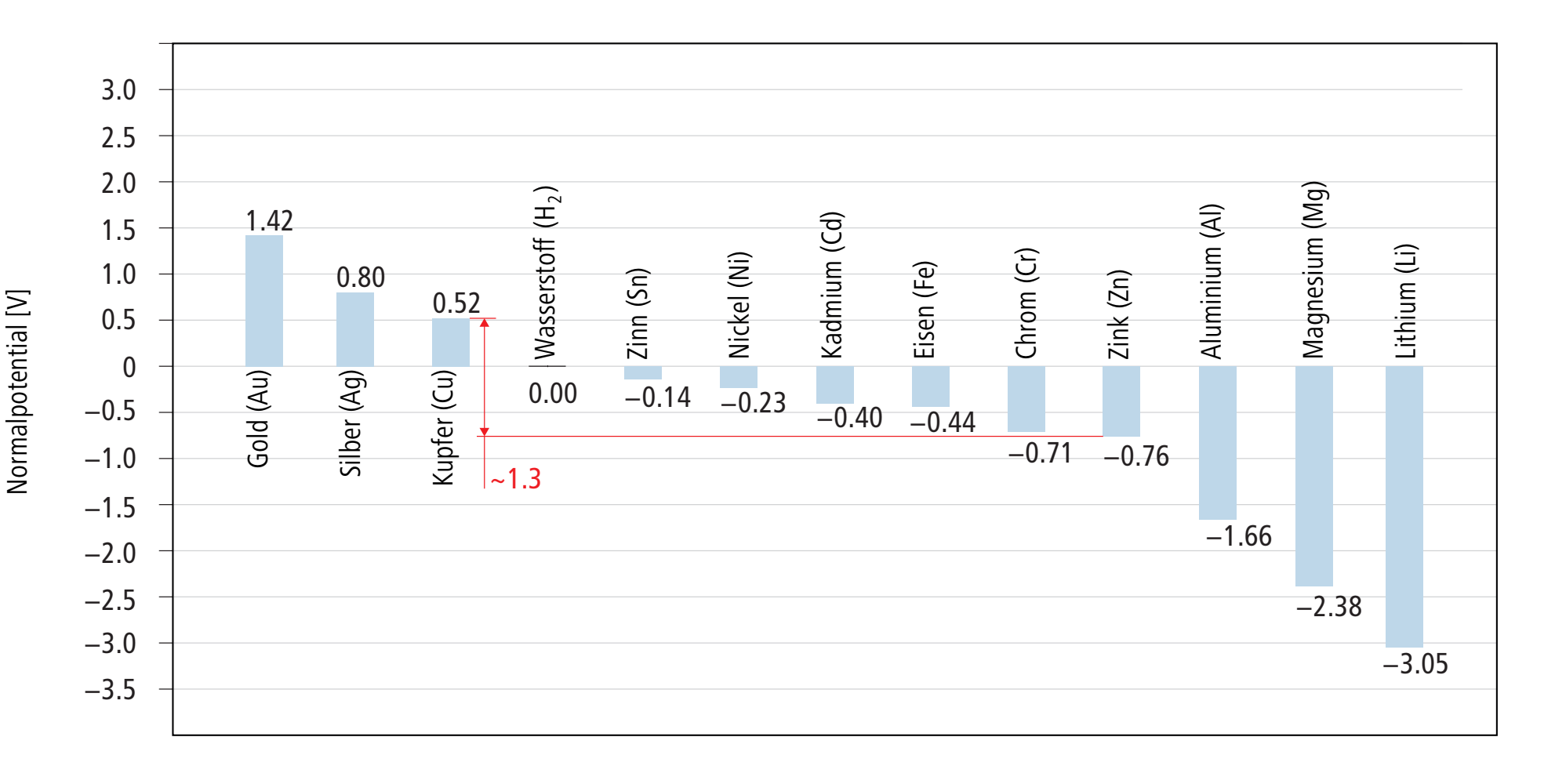
Die folgende Darstellung zeigt die Normalpotentiale von einigen Elementen gegenüber der Normalwasserstoffelektrode.
Um die Potentialdifferenz von zwei Werkstoffen zu bestimmen, die zusammen ein galvanisches Element bilden, wird die Differenz von deren Potentialen berechnet. Zum Beispiel beträgt die Potentialdifferenz zwischen einer Kupfer- und einer Zinkelektrode gemäss obiger Darstellung ungefähr 1.3 Volt.
Die folgende Tabelle zeigt die Potentiale von einigen in der Installationstechnik häufig verwendeten Werkstoffen, wobei die Potentiale der Metalle in Trinkwasser bezüglich einer Kupfersulfatelektrode gemessen wurden.
|
Werkstoff |
Potential E* [V] |
|---|---|
|
Kupfer |
−0.10 |
|
Nichtrostender Stahl |
−0.10 |
|
Rotguss und Si-Bronze |
−0.20 |
|
Messing |
−0.35 |
|
Eisen |
−0.55**/−0.75*** |
|
Stahl verzinkt |
−0.75 |
|
* in Trinkwasser bezüglich einer Kupfersulfatelektrode ** Trinkwasser belüftet *** Trinkwasser stagnierend |
|
Elektrochemische Spannungsreihe (nach suissetec Merkblatt W10018)
2.5 Galvanische Elemente
Zwischen zwei Elektroden mit unterschiedlichem Potential, die in einen Elektrolyten eingetaucht sind, kann eine Potentialdifferenz gemessen werden. Diese Spannung bewirkt bei geschlossenem Stromkreis einen Strom. Eine solche Anordnung wird als galvanisches Element, galvanische Zelle oder kurz als Element bezeichnet.
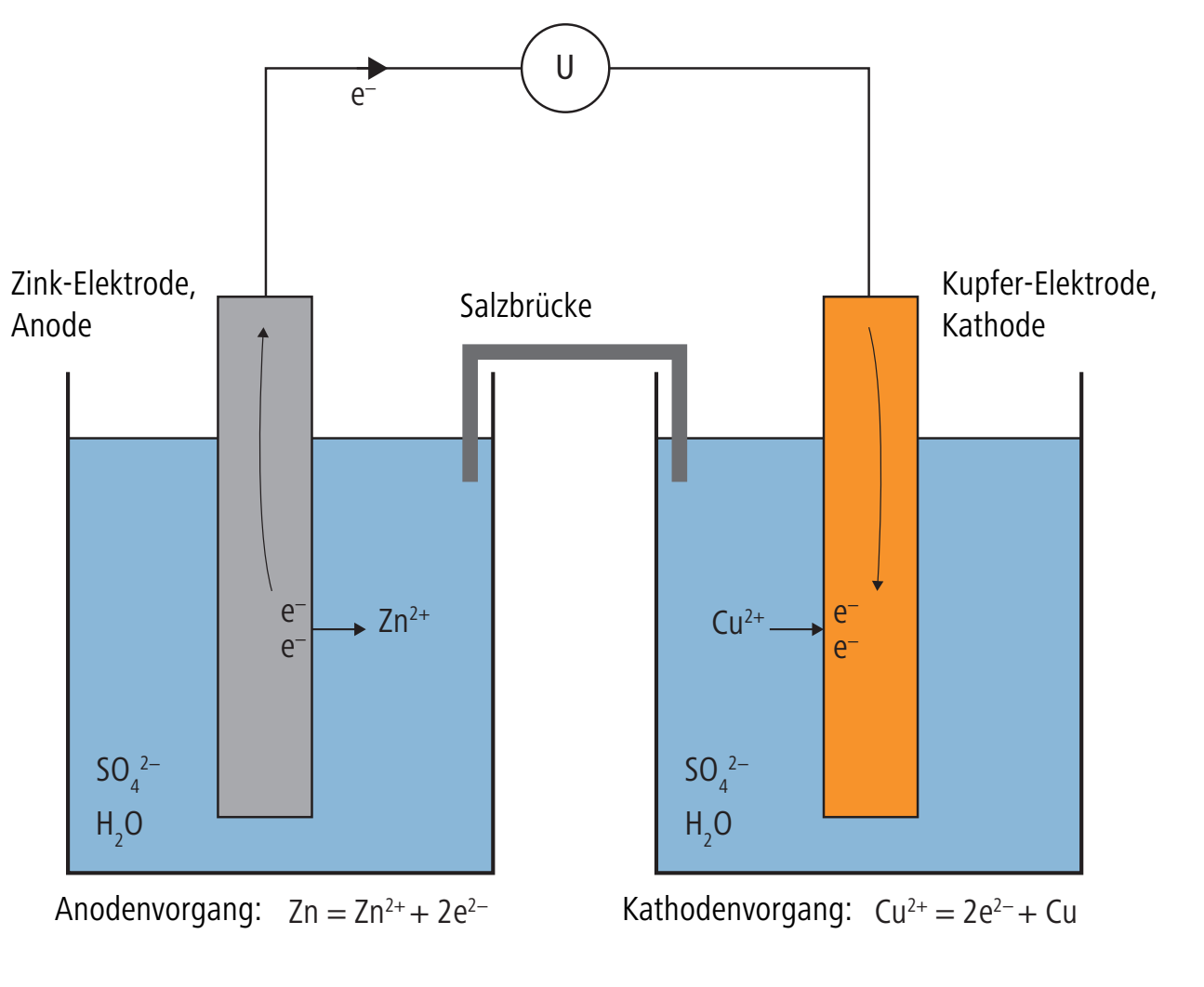
In der Geschichte der Elektrochemie ist das Daniell-Element wichtig, da es auch die historische Basis der heutigen Definition der Einheit der elektrischen Spannung ist. Das Daniell-Element besteht aus eine Kupfer-Elektrode und einer Zink-Elektrode. Die Kupfer-Elektrode ist in einer Kupfersulphat-Lösung, die Zink-Elektrode in eine Zinksulfatlösung eingetaucht. Beide Lösungen befinden sich in getrennten Behältern, damit sie sich nicht vermischen. Die Salzbrücke ermöglicht den Durchgang von Ionen und somit den Stromfluss.
An der Zink-Elektrode geht Zink in Lösung. Dadurch werden Elektronen frei, die als elektrischer Strom zur Kupfer-Elektrode fliessen, wo es zur Abscheidung von Kupfer kommt. Der Strom fliesst solange, bis die Zink-Elektrode vollständig aufgelöst ist.
Die Berechnung des Potentials des Daniell-Elements mithilfe der Nernst-Gleichung ergibt einen Wert von 1.1 Volt.
2.6 Korrosionsstrom und Flächenregel
Der Korrosionsstrom wird durch die elektrochemische Potentialdifferenz und weiteren Einflussgrössen bestimmt:
-
Zusammensetzung und Eigenschaften des Elektrolyten, z. B. Leitfähigkeit, pH-Wert, Sauerstoffgehalt, Salzgehalt und Temperatur.
-
Umgebungsbedingungen wie Luftfeuchtigkeit, aggressive, korrosive Stoffe in der Luft
-
Eventuell vorhandenen Passivschichten oder Beschichtungen
Die Korrosionsstromdichte bestimmt die Korrosionsgeschwindigkeit. Eine hohe Korrosionsstromdichte bewirkt eine schnellere Korrosion des unedlen Metalls. Je kleiner die Fläche des unedlen Metalls im Verhältnis zur Fläche des edlen Metalls ist, desto grösser ist die Korrosionsstromdichte. Dies wird mit der folgenden Formel ausgedrückt:
|
Formelzeichen |
Einheit |
Beschreibung |
|---|---|---|
|
İMe |
[A] |
Anodenstrom |
|
IOx |
[A] |
Kathodenstrom |
|
AK |
[m2] |
Kathodenfläche |
|
AA |
[m2] |
Anodenfläche |
Die Korrosionsgeschwindigkeit ist proportional zum Anodenstrom, d. h. je grösser der Anodenstrom, desto höher ist die Korrosionsgeschwindigkeit. Das Minus-Zeichen in der Formel ist darauf zurückzuführen, dass Anodenstrom und Kathodenstrom vom Betrag her gleich gross sind und bezüglich einem Knotenpunkt im Stromkreis in entgegengesetzter Richtung fliessen (Summe der Teilströme in einem geschlossenen Stromkreis ist gleich Null).
Das folgende Bild zeigt eine schematische Darstellung der Flächenregel:

2.7 Kategorien atmosphärischer Korrosion
Die atmosphärische Korrosion bezeichnet die Korrosion von Werkstoffen mit der Erdatmosphäre als Korrosionsmedium bei Umgebungstemperatur. Nach EN ISO 12944-2 werden atmosphärische Umgebungen in Kategorien atmosphärischer Korrosivität eingeteilt.
|
Korrosivitätskategorie |
Beispiele typischer Umgebungen (nur informativ) |
|
|---|---|---|
|
Freiluft |
Innenraum |
|
|
C1 unbedeutend |
— |
Beheizte Gebäude mit neutraler Atmosphäre, z. B. Büros, Verkaufsräume, Schulen, Hotels |
|
C2 gering |
Atmosphäre mit geringem Verunreinigungsgrad: meistens ländliche Gebiete |
Unbeheizte Gebäude, in denen Kondensation auftrteten kann, z. B. Lagerhallen, Sporthallen |
|
C3 mässig |
Stadt- und Industrieatmosphäre mit mässiger Schwefeldioxidbelastung; Küstenatmosphäre mit geringer Salzbelastung |
Produktionsräume mit hoher Luftfeuchte und gewisser Luftverunreinigung, z. B. Lebensmittelverarbeitungsanlagen, Wäschereien, Brauereien, Molkereien |
|
C4 stark |
Industrieatmosphäre und Küstenatmosphäre mit mässiger Salzbelastung |
Chemieanlagen, Schwimmbäder, küstennahe Werften und Bootshäfen |
Korrosivitätskategorien nach EN ISO 12944-2:2017
Die folgende Tabelle enthält eine Liste der in der Sanitärtechnik häufig verwendeten Werkstoffe und Beschichtungen sowie deren Beständigkeit in Atmosphären gemäss den Korrosivitätskategorien nach EN ISO 12944-2:2017.
|
Korrosivitätskategorie |
Werkstoffe und Beschichtungen |
||
|---|---|---|---|
|
Stahl verzinkt |
Edelstahl |
Kunststoffe |
|
|
C1 unbedeutend |
|
|
|
|
C2 gering |
Zusätzliche Schutzmassnahme erforderlich, z. B. Kunststoffbeschichtung oder Schutzschlauch |
|
|
|
C3 mässig |
Zusätzliche Schutzmassnahme erforderlich, z. B. Kunststoffbeschichtung oder Schutzschlauch |
|
|
|
C4 stark |
Zusätzliche Schutzmassnahme erforderlich, z. B. Kunststoffbeschichtung oder Schutzschlauch |
Zusätzliche Schutzmassnahme erforderlich, z. B. Kunststoffbeschichtung oder Schutzschlauch |
|
Beständigkeit von Rohrwerkstoffen in Atmosphären nach EN ISO 12944-2:2017